Введение
Гиперадренокортицизм или синдром Кушинга у собак – это заболевание, сопровождающееся повышенным уровнем кортизола в крови. По некоторым данным, у собак мелких пород чаще всего встречается гипофизарный гиперадренокортицизм, в то время как у крупных животных – надпочечниковый гиперадренокортицизм. Также некоторые авторы утверждают6, что в случае гипофизарного гиперадренокортицизма половая предрасположенность не выявлена, а надпочечниковый гиперадренокортицизм чаще встречается у сук крупных пород6, и болеют преимущественно собаки среднего и старшего возраста. Вне зависимости от этиологии гиперадренокортицизма в клинической практике мы будем сталкиваться с мощным катаболическим эффектом кортизола, который постепенно разрушает все органы и ткани. Конечно, если речь идет о гипофизарном гиперадренокортицизме, можно столкнуться с неврологической симптоматикой (вестибулярным синдромом, «упиранием» головой в стену) при наличии макроаденомы гипофиза и, возможно, со снижением аппетита по этой причине. Однако чаще всего при классическом течении гиперадренокортицизм сопровождается повышенным аппетитом, полиурией и полидипсией с сохранением активности6-8.В данной статье речь пойдет о гипофизарном гиперадренокортицизме у кобеля породы китайская хохлатая собака.
Клинический случай
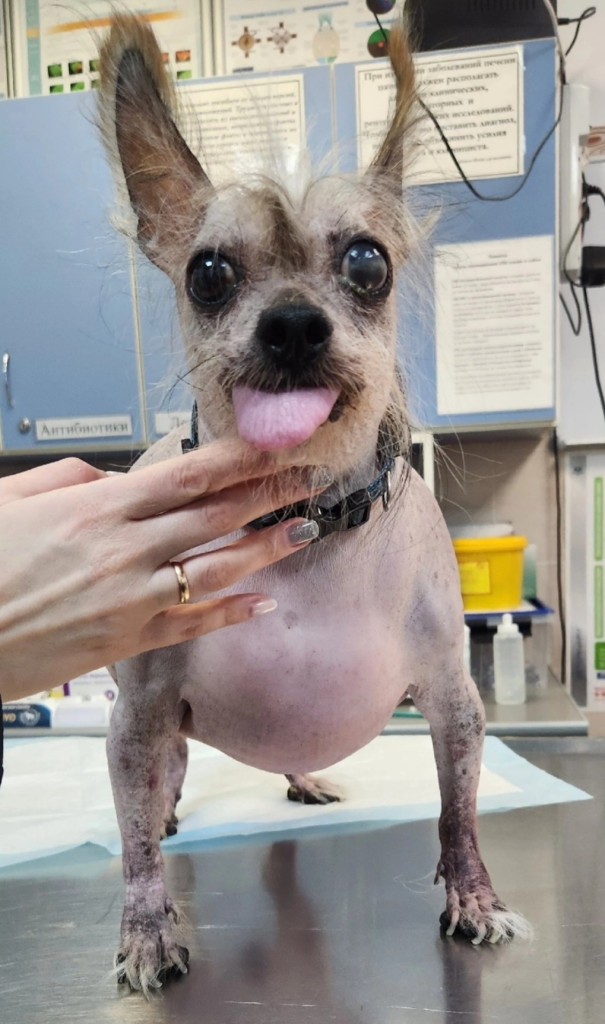
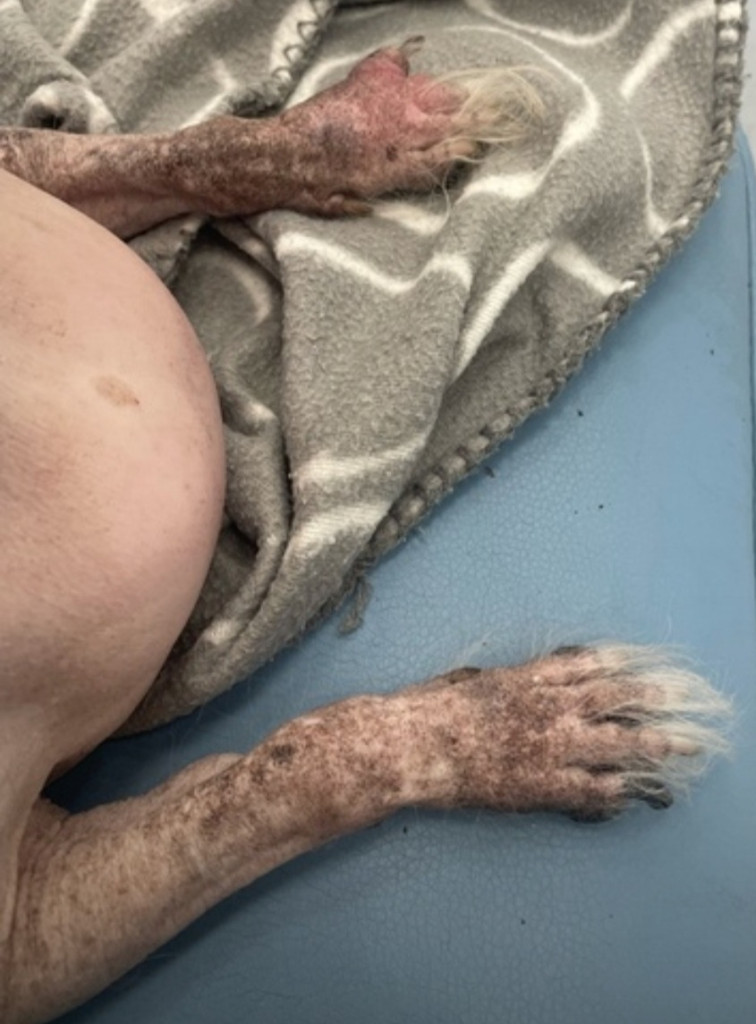
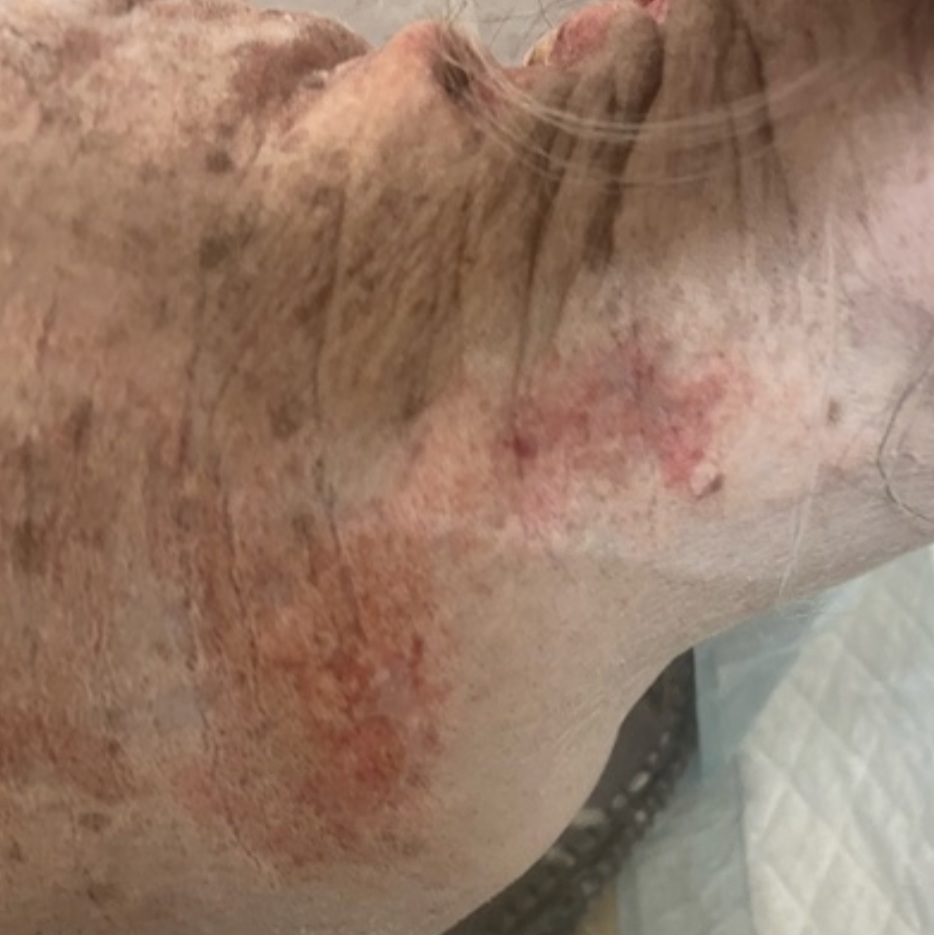
Пациент: 10-летний кобель по кличке Кузя, ревакцинированный, дегельминтизированный. По словам владельцев, в течение последних двух лет питомец начал очень быстро набирать вес и ослеп на один глаз. Возможно, из-за лишнего веса «почти совсем отказывают лапы», собака хромает, часто лижет пальцы и стала сильно храпеть. Кроме того, примерно в течение двух лет присутствовали полифагия, полиурия, полидипсия. Неврологических симптомов владельцы не замечали, а обратились на прием к ортопеду по причине хромоты, ортопед же в свою очередь рекомендовал обратиться к эндокринологу, заподозрив у собаки сахарный диабет (фото 1).Результат первичного осмотра у эндокринолога. Вес пациента составил 9 кг, температура 38 °C, среднее артериальное давление – 119/90 мм рт. ст. Выявлено наличие хромоты, эритемы конечностей, избыточной массы тела и телеангиэктазии (фото 2).
На основании данных осмотра и анамнеза был поставлен предварительный диагноз «гиперадренокортицизм»1.
Все вышеперечисленные симптомы и данные осмотра являются следствием негативного воздействия кортизола, секретируемого в избыточном количестве, на организм собаки, а именно:
- повышение скорости клубочковой фильтрации почек4 и нарушение действия антидиуретического гормона на уровне собирательных почечных канальцев приводят к полиурии/полидипсии;
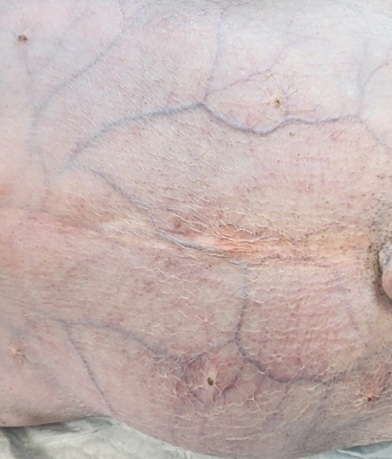
- за счет усиленного катаболизма белков уменьшение транспорта белков в органы и ткани приводит к истончению и сухости кожи, вследствие чего вены визуализируются более отчетливо;
- кожа истончается, сосудистая сеть хорошо визуализируется из-за ингибирования продукции основной субстанции, коллагена и пролиферации фибробластов;
- развиваются мышечная гипотрофия, слабость, происходит растяжение связок и сухожилий, соответственно, хромота развивается не только за счет лишнего веса, но и за счет растяжения мышечной ткани, связок и сухожилий9.
Дексаметазоновая проба и визуальная диагностика являются методами постановки окончательного диагноза «гиперадренокортицизм». Клинический и биохимический анализы крови считаются золотым стандартом базовой диагностики при любых заболеваниях у животных, а дексаметазоновая проба позволяет выявить ответ надпочечников на экзогенное введение дексаметазона и, таким образом, подтвердить или опровергнуть диагноз «синдром Кушинга».
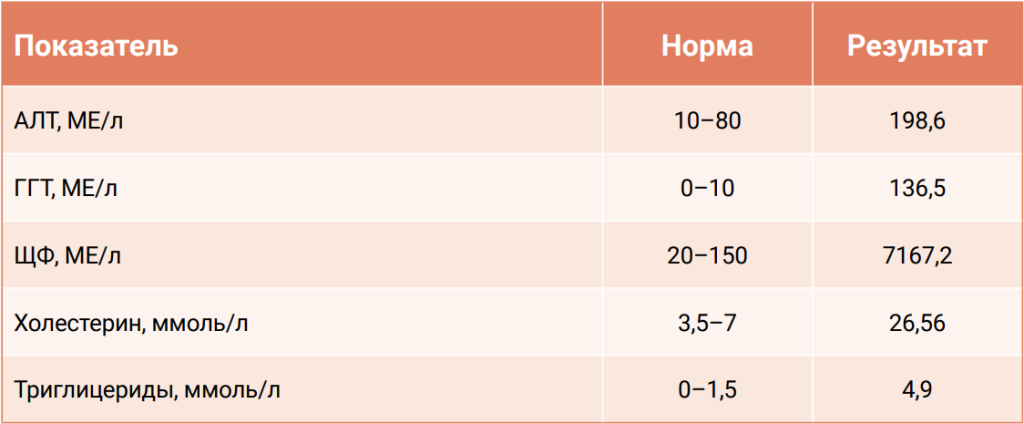
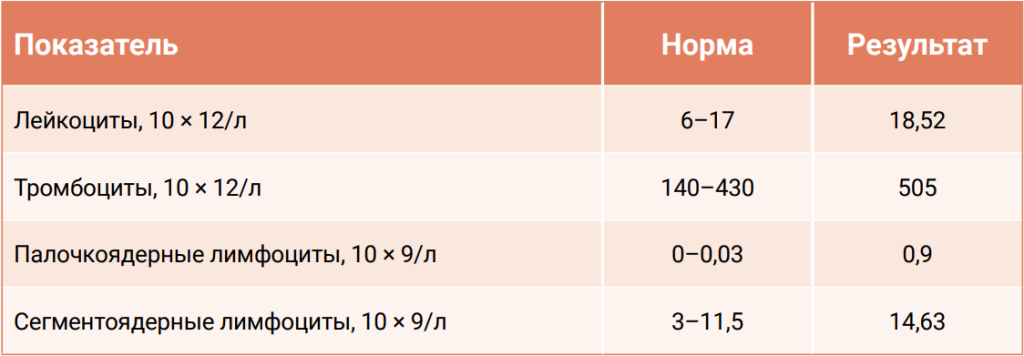
Результаты анализов отражены в таблицах 1, 2 (представлены только показатели, превышающие референтный интервал).
По результатам проведенных исследований были выявлены характерные биохимические изменения в сыворотке крови: повышение печеночных трансаминаз, показателей липидного обмена2.
В клиническом анализе крови был выявлен лейкоцитоз, что также является характерной находкой для данного заболевания.
Малая дексаметазоновая проба оказалась положительной: отсутствие супрессии синтеза кортизола через 8 часов после введения дексаметазона (график 1). Таким образом, при введении дексаметазона надпочечники продолжают вырабатывать кортизол в большом количестве, что является характерным для наличия новообразования, секретирующего кортизол или АКТГ в избыточном количестве.
УЗИ. При проведении ультразвукового исследования брюшной полости были выявлены симметричная гиперплазия надпочечников, кальцинаты селезенки, сладж желчного пузыря.
Симметричная гиперплазия надпочечников характерна для гипофизарного гиперадренокортицизма, поскольку секретируемый в избыточном количестве опухолью гипофиза адренокортикотропный гормон (АКТГ) оказывает системное влияние. Для оценки размеров новообразования гипофиза необходимо было сделать МРТ головного мозга, но владельцы Кузи отказались от проведения данного исследования и последующего лечения собаки.
По нашим наблюдениям, макроаденома гипофиза может сопровождаться неврологической симптоматикой, а также привести к снижению аппетита.
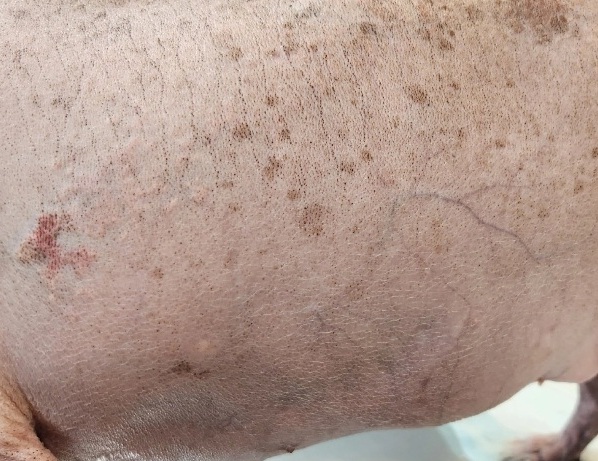
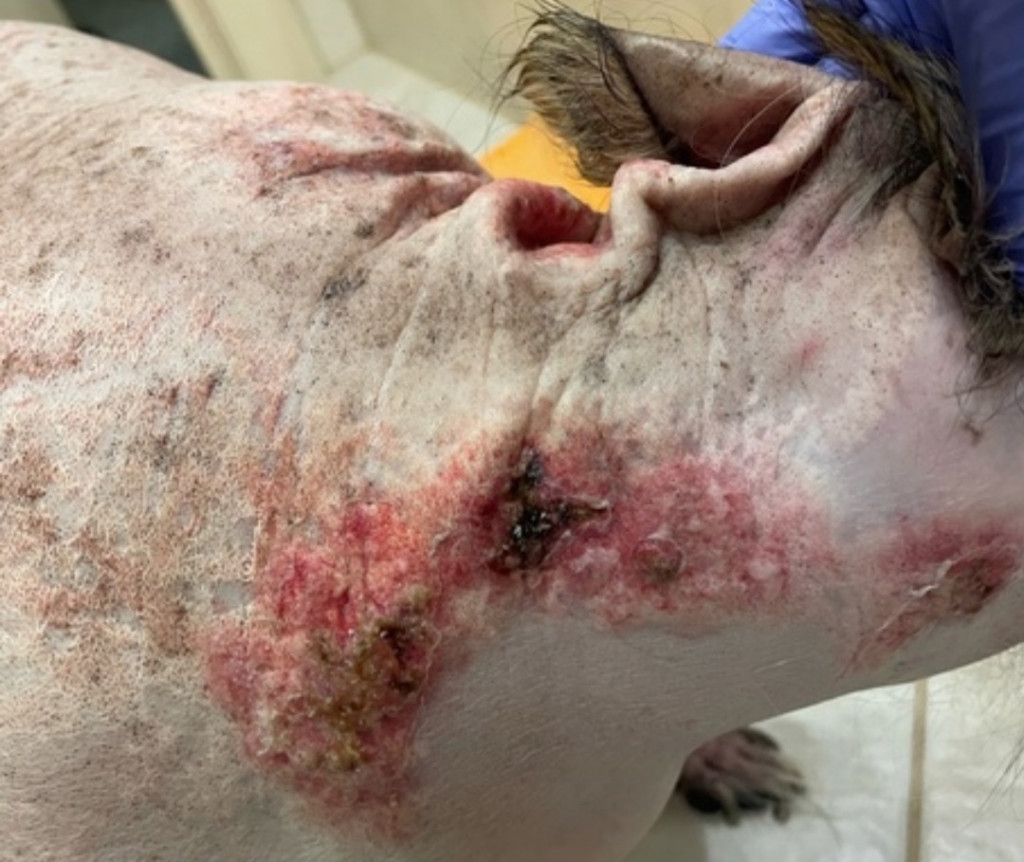
Далее в течение месяца после первичного приема у собаки стали прогрессировать симптомы гиперадренокортицизма, развился выраженный кальциноз кожи (фото 3) с присоединением вторичной бактериальной микрофлоры. Также прогрессировала хромота, значительно ухудшалось качество жизни собаки, однако при этом аппетит был сохранен. В связи с ухудшением состояния питомца владельцы приняли решение о проведении эвтаназии.
Как правило, собаки с гиперадренокортицизмом без лечения могут жить относительно долго с сохранением аппетита, пока не разовьются симптомы, значительно ухудшающие качество жизни животного. Симптомы могут быть весьма разнообразными: неврологические нарушения, вызванные макроаденомой гипофиза; тяжелые поражения кожи – кальциноз; слабость конечностей, хромота, болезненность, которые развиваются вследствие катаболического действия кортизола. Только своевременно подобранное лечение позволит контролировать симптомы, обеспечивать контроль заболевания и улучшить качество жизни.
Обсуждение
Кузе был назначен препарат «Веторил» (основное действующее вещество – трилостан) – 10 мг (1 мг/кг) по 1 капсуле 2 раза в день с едой для медикаментозного контроля гиперадренокортицизма. Также допустимым вариантом применения трилостана является доза2 мг/кг 1 раз в сутки3. Помимо трилостана, для лечения синдрома Кушинга может назначаться препарат «Митотан», однако Кузе был назначен трилостан, поскольку, согласно данным, он обладает менее выраженными побочными эффектами по сравнению с митотаном3.
Оценку результатов лечения было рекомендовано осуществлять посредством проведения исследования крови на биохимические показатели, электролиты и стимулирующей пробы с АКТГ через 10 дней, 4 недели, 12 недель, а затем каждые 3 месяца с момента начала терапии6. Однако, как правило, наиболее полное действие препарата проявляется через 4 недели с момента начала терапии. Контроль результатов лечения необходим в первую очередь для исключения передозировки и развития ятрогенного гипоадренокортицизма9.
Трилостан эффективен как при гипофизарном, так и при надпочечниковом гиперадренокортицизме (однако необходимо помнить о том, что применение трилостана не будет способствовать разрушению опухоли надпочечника), он ингибирует выработку преимущественно глюкокортикостероидов, а также минералокортикоидов и половых гормонов3.
При постановке диагноза «синдром Кушинга» врачу необходимо выявить этиологию заболевания и взвесить пользу и возможные риски развития побочных эффектов от назначенного лечения, а также проинформировать владельцев о возможных последствиях в случае их отказа от лечения питомца. Клинический случай Кузи интересен именно тем, что наглядно демонстрирует прогрессирование симптомов при отсутствии лечения.
Собаки с гиперадренокортицизмом без лечения могут жить относительно долго до наступления значимого ухудшения качества их жизни. У Кузи симптом кальциноза кожи прогрессировал быстро при отсутствии лечения (всего за 1 месяц с момента первичного приема), что приводило к выраженной болезненности, кроме того, также прогрессировала хромота – все это послужило причиной принятия владельцами решения об эвтаназии питомца.
У данного пациента присутствовали типичные клинические признаки гиперадренокортицизма: полиурия, полидипсия, полифагия, ожирение. Однако в редких случаях у таких собак может также развиваться кахексия и гипотрофия мышечной массы10. Несмотря на характерные симптомы заболевания, врач должен грамотно дифференцировать гиперадренокортицизм и гипотиреоз у собак, а в некоторых случаях данные заболевания могут протекать параллельно у одного животного. Особенно затруднительно проводить дифференциальную диагностику при подозрении на развитие синдрома эутиреоидной слабости5. Для постановки диагноза применяются как лабораторные методы исследования, описанные выше, так и методы визуальной диагностики, поскольку развитие гиперадренокортицизма провоцирует возникновение опухоли, которая находится либо в надпочечнике/ах, либо в передней доле гипофиза. Сложность диагностики может быть связана с доступностью и качеством оборудования для проведения визуальной диагностики, а также с опытом ветеринарного врача при интерпретации результатов дексаметазоновых проб и анализов крови.
Лечение данного заболевания можно проводить консервативно препаратами, которые способны подавлять функцию коры надпочечников (наиболее эффективны трилостан и митотан)1,2. При проведении данной терапии возможно развитие ятрогенного гипоадренокортицизма, что потребует отдельной коррекции состояния.
Хирургическое удаление новообразования надпочечника либо гипофиза связано с анестезиологическими рисками. Важно отметить, что новообразование правого надпочечника сложнее поддается хирургическому лечению, так как правый надпочечник расположен ближе к каудальной полой вене (сосуд с низкой скоростью кровотока), следовательно, новообразование правого надпочечника часто прорастает в каудальную полую вену, в то время как левый надпочечник располагается рядом с аортой (сосудом с высокой скоростью кровотока), соответственно, реже в нее прорастает.
Таким образом, выбор тактики лечения при диагнозе «гиперадренокортицизм» требует тщательного и индивидуального подхода к каждому пациенту. Ветеринарный врач и владелец должны принимать решение совместно, учитывая потенциальную пользу, риски и стоимость лечения.
Литература:
- Audrey Cook. The Diagnosis of Canine Hyperadrenocorticism. ссылка
- Nagata N., Kojima K., Yuki M. Comparison of Survival Times for Dogs with Pituitary-Dependent Hyperadrenocorticism in a Primary-Care Hospital: Treated with Trilostane versus Untreated, 2016. DOI: 10.1111/jvim.14617
- Areas С., Melian C. Long-term survival of dogs with adrenal-dependent hyperadrenocorticism: a comparison between mitotane and twice daily trilostane treatment, 2014. DOI: 10.1111/jvim.12303
- Baas J. J., Schaeffer F., Joles J. A. The influence of cortisol excess on kidney function in the dog, 1984.
- Гусева В. А. Дифференциальная диагностика гипотиреоза собак и синдрома эутиреоидной слабости. Ветеринарный Петербург, № 3 – 2020.
- Игнатенко Н. А. Гиперадренокортицизм: диагностика и лечение у собак. VetPharma, № 6 –2012.
- Леметайнер Д., Блуа Ш. Обновленная информация о применении трилостана у собак. Ветеринарный Петербург, № 2 – 2024 ссылка
- Смирнова О. О. Обзор частных отклонений в результатах рутинных лабораторных тестов у собак с гиперадренокортицизмом. ссылка
- Смирнова О. О. Спонтанный гиперадренокортицизм у собак: терапевтическое лечение трилостаном. – Современная ветеринарная медицина, № 6 – 2021. ссылка
- Гиперадренокортицизм собак. ссылка

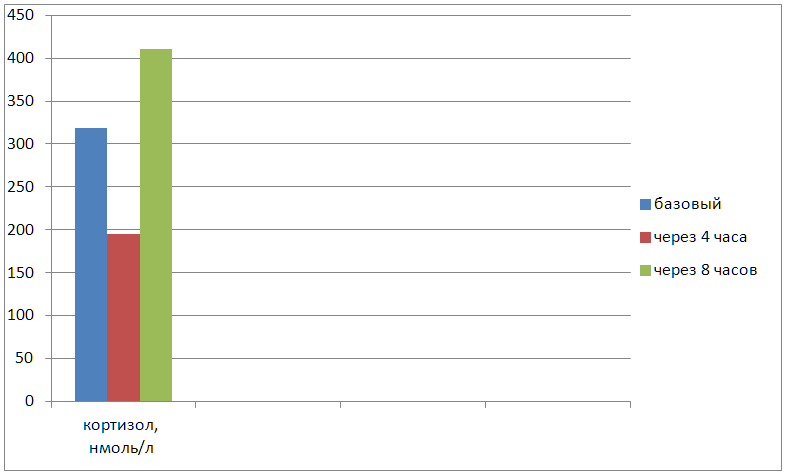
 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург