Первичный гиперальдостеронизм – это эндокринное заболевание, характеризующееся избыточной секрецией альдостерона корой надпочечников. Впервые это состояние было описано у кошки в 1983 году, однако его диагностика остается сложной задачей из-за низкой распространенности и неспецифичности клинических проявлений. Тем не менее первичный гиперальдостеронизм считается одним из наиболее частых эндокринных нарушений надпочечников у кошек3.
Вторичный гиперальдостеронизм представляет собой патологическое состояние, обусловленное активацией ренин-ангиотензин-альдостероновой системы (РААС), например при снижении объема циркулирующей крови (гиповолемии) для увеличения реабсорбции натрия и воды.
Этиология. Первичный гиперальдостеронизм характеризуется избыточной секрецией альдостерона, обусловленной опухолевым поражением коры надпочечников (как правило, аденомой или аденокарциномой, поражающей один надпочечник, реже – оба). В ряде случаев первичный гиперальдостеронизм может иметь идиопатическую природу, при которой наблюдается гиперплазия клубочковой зоны коры надпочечников.
Вторичный гиперальдостеронизм развивается на фоне сердечной, печеночной и почечной недостаточности, при активации ренин-ангиотензин-альдостероновой системы (РААС), а также при дефиците натрия в рационе12.
Физиология и патофизиология
Для понимания патогенеза симптомов гиперальдостеронизма необходимо рассмотреть функции альдостерона. Альдостерон является минералокортикоидным гормоном, синтезируемым клубочковой зоной коры надпочечников. Его секреция регулируется ренин-ангиотензин-альдостероновой системой (РААС), которая играет центральную роль в регуляции артериального давления. Снижение артериального давления вызывает активацию юкстагломерулярных клеток артериол почечных клубочков, что приводит к секреции протеолитического фермента ренина в кровь и лимфу. Ренин воздействует на белок ангиотензиноген, способствуя его преобразованию в ангиотензин I. Далее ангиотензин I под влиянием ангиотензинпревращающего фермента трансформируется в ангиотензин II. Ангиотензин II, в свою очередь, вызывает вазоконстрикцию сосудов, стимулирует секрецию вазопрессина гипофизом, адреналина и норадреналина – надпочечниками, а также усиливает выработку альдостерона корой надпочечников. При развитии первичного гиперальдостеронизма новообразование надпочечника(ов) или гиперплазированная кора надпочечников секретирует избыточное количество альдостерона автономно, независимо от системы РААС. Циркулирующий альдостерон воздействует на ткани почек, толстой кишки и слюнных желез и проходит через плазматические мембраны этих эпителиальных клеток, связываясь с цитоплазматическими минералокортикоидными рецепторами. Альдостерон выполняет ряд важнейших функций в организме: усиливает канальцевую реабсорбцию натрия и секрецию калия канальцевым эпителием почек. В ответ на альдостерон эпителиальные клетки дистальных извитых канальцев и собирательных трубочек увеличивают реабсорбцию натрия, что приводит к задержке воды. Объем плазмы и внеклеточной жидкости увеличивается вместе с общим периферическим сопротивлением из-за сужения сосудов под действием ангиотензина II, что приводит к повышению артериального давления. Таким образом, альдостерон способствует транспорту натрия и воды во внутриклеточное пространство, из-за чего увеличивается объем циркулирующей крови и повышается артериальное давление4.Важно помнить о том, что артериальная гипертензия, гипокалиемия или их сочетание часто является следствием хронической болезни почек (ХБП). Было установлено, что первичный гиперальдостеронизм усугубляет прогрессирование ХБП, действуя как посредник. ХБП характеризуется повреждением клубочков, тубулоинтерстициальной ткани и избыточным накоплением внеклеточного матрикса в почках. Накопление внеклеточного матрикса может быть обусловлено влиянием различных факторов роста и ангиотензином II. Их действие может быть связано с усилением гиперплазии или гипертрофии мезангиальных, эндотелиальных, тубулярных эпителиальных и интерстициальных фибробластов почек. Ангиотензин II, помимо своего периферического сосудосуживающего действия, является важным регулятором клубочковой фильтрации и ключевым фактором в патогенезе ХБП. Альдостерон также играет значительную роль в прогрессировании почечных повреждений, способствуя развитию тромбоза и фиброза сосудов. Взаимодействие ангиотензина II и альдостерона приводит к поддержанию системной гипертензии и дальнейшему фиброзно-пролиферативному разрушению почечной ткани. Важно понимать, какую роль эти факторы играют в прогрессировании заболеваний почек, поскольку системная гипертензия, гипокалиемия и их сочетание у пожилых кошек часто являются клиническими признаками ХБП как основного заболевания, а не прямым следствием первичного гиперальдостеронизма. В связи с этим перед клиницистом встает сложная задача дифференциации первичной патологии и определения основного этиологического фактора гипокалиемии и системной артериальной гипертензии: первичного гиперальдостеронизма или ХБП. У кошек с исходно нормальной функцией почек или легкой азотемией может наблюдаться прогрессирование почечной патологии, поскольку гиперальдостеронизм может привести к гломерулярному склерозу, атрофии канальцев, гиалиновому склерозу артериол и интерстициальному фиброзу12. Артериальная гипертензия в основном является результатом увеличения объема циркулирующей крови из-за опосредованной альдостероном задержки натрия и жидкости, а увеличение внеклеточного объема, в свою очередь, приводит к увеличению сердечного выброса. Недавно было зарегистрировано воздействие альдостерона на сосудистый тонус и ремоделирование сосудов, приводящее к дисфункции их эндотелия. Артериальную гипертензию при первичном гиперальдостеронизме следует рассматривать как многофакторный процесс, на который влияют увеличение внеклеточного объема, повышенная симпатическая активность и повышение системного сосудистого сопротивления. Результаты исследований лабораторных животных показали, что ткани сердца продуцируют 1% альдостерона от его общего количества, вырабатываемого надпочечниками. Это способствует его участию в развитии эссенциальной гипертензии и вторичного гиперальдостеронизма у пациентов с сердечной недостаточностью за счет увеличения секреции альдостерона и повышения чувствительности к нему клеток-мишеней. Длительно протекающая артериальная гипертензия может приводить к концентрической гипертрофии левого желудочка у людей и у кошек, что подтверждает гипотезу о воздействии альдостерона непосредственно на кардиомиоциты1.
Клинические признаки
Первичный гиперальдостеронизм не имеет специфических клинических признаков и может восприниматься врачами и владельцами животных как естественные изменения в гериатрическом возрасте. В связи с этим важно разработать и строго соблюдать четкий алгоритм действий при подозрении на данное заболевание для своевременной диагностики и лечения.Симптомы вторичного гиперальдостеронизма зависят от основного заболевания. Сложность диагностики обусловлена тем, что на ранних стадиях заболевания гипокалиемию и артериальную гипертензию сложно распознать, а также эти симптомы не являются патогномоничными для первичного гиперальдостеронизма. На основании опубликованных данных выявлено, что более чем у 90% кошек с первичным гиперальдостеронизмом наблюдалось значительное повышение систолического артериального давления (более 160 мм рт. ст.), тогда как у людей системная артериальная гипертензия при первичном гиперальдостеронизме проявляется лишь в 5–12% случаев10. Артериальная гипертензия также может быть выявлена как в процессе проведения рутинных клинических исследований, так и при появлении характерных клинических признаков, связанных с прогрессированием гипертензии, таких как слепота, развившаяся вследствие отслоения сетчатки, гифема. Согласно некоторым данным, гиперплазия надпочечников у кошек ассоциируется с более выраженным повышением артериального давления по сравнению с опухолями надпочечников12. При первичном гиперальдостеронизме у кошек развивается гипокалиемия, что приводит к мышечной слабости. Клинические проявления варьируются от трудно диагностируемой апатии до стопохождения и вентрофлексии при прогрессировании заболевания.
Сложность диагностики заключается в том, что начальные симптомы, такие как апатия и летаргия, владельцем животного и врачом могут быть ошибочно приняты за признаки старения животного, и только при появлении патогномоничных признаков гипокалиемии (вентрофлексия и стопохождение) можно заподозрить первичный гиперальдостеронизм.
У кошек с гиперальдостеронизмом не всегда наблюдаются классические признаки, связанные с гипокалиемией или гипертензией. На первичном приеме может быть выявлено только одно из этих отклонений или их отсутствие. Среди менее специфических симптомов можно выделить полиурию и компенсаторную полидипсию, обусловленные хронической гипокалиемией, которая нарушает концентрирующую функцию почек; кахексию; пальпируемые образования в брюшной полости; полифагию, а также ухудшение качества шерсти и шумы в проекции клапанов сердца (иногда с нарушением ритма)4.
Диагностика
Любая кошка, у которой наблюдаются клинические признаки системной артериальной гипертензии, гипокалиемии +/– умеренной азотемии, должна быть обследована на предмет возможного наличия первичного гиперальдостеронизма.Хотя гипертензия и гипокалиемия являются наиболее распространенными отклонениями, отсутствие одного из этих отклонений не исключает наличия заболевания.
Тщательный сбор анамнеза и физикальное обследование, проведение рутинных лабораторных исследований (общий и биохимический анализы крови, определение уровня Т4 общего, анализ мочи) помогут исключить большинство других причин гипокалиемии и гипертензии.
При появлении клинических признаков, позволяющих предположить наличие гиперальдостеронизма, необходимо провести комплексное диагностическое обследование.
Важным этапом является УЗИ или КТ надпочечников для выявления возможных новообразований. В норме продольный размер надпочечников у кошек составляет 10–11 мм, а максимальный диаметр – 4,3 ± 0,3 мм8. Однако следует учитывать, что наличие новообразований в надпочечнике(ах) не всегда свидетельствует о первичном гиперальдостеронизме, поскольку они могут быть гормонально неактивными (инциденталомы).
Для подтверждения диагноза «гиперальдостеронизм» необходимо провести лабораторную диагностику. Без результатов лабораторных исследований постановка точного диагноза невозможна.
Высокая концентрация альдостерона в плазме, особенно в сочетании с клиническими признаками, клинико-патологическими отклонениями и опухолью надпочечника, является индикатором первичного гиперальдостеронизма. Однако выявление высокой концентрации альдостерона в плазме само по себе не позволяет дифференцировать первичный и вторичный гиперальдостеронизм9,10.
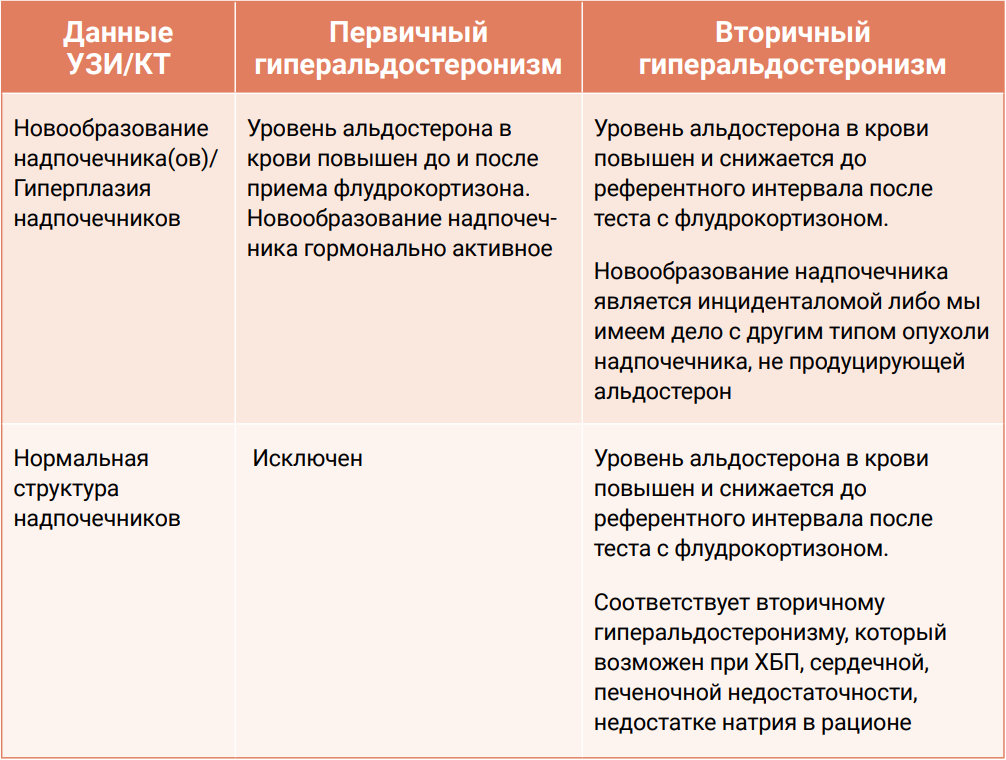
Интерпретацию концентрации альдостерона необходимо проводить в контексте уровня калия в плазме крови, так как в норме гипокалиемия должна подавлять высвобождение альдостерона клубочковой зоной коры надпочечников. В случае отсутствия гиперальдостеронизма при наличии гипокалиемии уровень альдостерона должен быть ниже референтного интервала. Если же при наличии гипокалиемии концентрация альдостерона находится в пределах или выше референтного диапазона, это подтверждает диагноз «первичный гиперальдостеронизм» (табл. 1), потому что данная ситуация свидетельствует о том, что надпочечник(и) синтезируют кортизол автономно, независимо от уровня калия в плазме крови.
Для дифференциации первичного и вторичного гиперальдостеронизма проводится лабораторное исследование определения активности ренина в плазме крови. При подавлении активности ренина плазмы в сочетании с высокими концентрациями альдостерона (или высоким соотношением альдостерон/ренин) подтверждается автономная секреция альдостерона (первичный гиперальдостеронизм), независимая от активности ренина. Однако этот анализ не всегда доступен для кошек. У кошек с адренокортикальной опухолью этот показатель (альдостерон/ренин–соотношение) обычно значительно повышен, поскольку высвобождение ренина полностью подавлено. У кошек с гиперплазией коры надпочечников это соотношение может быть менее выраженным, так как может сохраняться некоторая активность ренина. Если данный тест доступен, он считается золотым стандартом для диагностики первичного гиперальдостеронизма. Точность результатов зависит от сохранения активности ренина в процессе сбора и хранения образцов. Для проведения достоверного исследования требуются значительный объем крови (4 мл) и мгновенное замораживание отделенной плазмы5.
Достоверным способом диагностики первичного гиперальдостеронизма является проведение теста подавления флудрокортизоном. При выявлении повышения уровня альдостерона в крови кошек им назначают флудрокортизон в дозе 0,05 мг/кг 2 раза в день в течение 4 дней. При наличии первичного гиперальдостеронизма уровень альдостерона в плазме крови не снижается после курса приема флудрокортизона, так как надпочечник(и) секретируют гормон автономно7. Если же происходит подавление синтеза альдостерона, это указывает на вторичный гиперальдостеронизм, поскольку флудрокортизон обладает минералокортикоидной активностью, аналогичной альдостерону (табл. 2).
Тест на супрессию с использованием препарата «Телмисартан», блокатора рецепторов ангиотензина II, может быть полезен для диагностики первичного гиперальдостеронизма у кошек. Теоретически у здоровых кошек можно ожидать подавление секреции альдостерона в ответ на введение данного препарата. Однако у кошек с первичным гиперальдостеронизмом, характеризующимся автономной секрецией альдостерона, значительного подавления его секреции не ожидается. Несмотря на потенциальную полезность этого теста в диагностике первичного гиперальдостеронизма у кошек, требуется дальнейшее изучение его эффективности и точности, особенно в контексте дифференциальной диагностики идиопатического первичного гиперальдостеронизма6.
Типичные биохимические отклонения у кошек с гиперальдостеронизмом характеризуются умеренной или тяжелой гипокалиемией, при этом концентрация натрия может оставаться в пределах нормы или незначительно повышаться. Задержка натрия, обусловленная нарушением водно-электролитного баланса, приводит к снижению концентрации натрия в плазме крови и, вероятно, является причиной того, что уровень этого электролита редко повышается. Также у кошек с гипокалиемической полимиопатией обычно отмечается значительное повышение концентрации креатинкиназы в сыворотке крови. В исследовании с участием 13 кошек с первичным гиперальдостеронизмом средний уровень калия при проявлении клинических симптомов составил 2,5 мЭкв/л (контрольный диапазон 4–5,5 мЭкв/л), концентрация натрия колебалась от 148 до 168 мЭкв/л (контрольный диапазон 140–160 мЭкв/л), наблюдалось серьезное повышение уровня креатинкиназы – среднее значение составило 6837 МЕ/л (контрольный диапазон < 120 МЕ/л), а у 12 из 13 животных была выявлена артериальная гипертензия (систолическое давление ≥ 170 мм рт. ст.)6.
Избыток альдостерона может привести к умеренному гипокалиемическому метаболическому алкалозу. У больных кошек может развиться гипофосфатемия, гипомагниемия.
Примечательно, что даже на терминальной стадии почечной недостаточности в сочетании с первичным гиперальдостеронизмом наблюдается тенденция к гипофосфатемии, а не к гиперфосфатемии11. Гипофосфатемия в таких случаях обусловлена тем, что длительная артериальная гипертензия, повреждающая почки, стимулирует секрецию паратиреоидного гормона под воздействием альдостерона. Это приводит к увеличению экскреции фосфора с мочой. Гипомагниемия часто сопровождает активацию РААС2.
Гистопатологические изменения в почках кошек могут быть такими же, как у людей с гиперальдостеронизмом: гиалиновый артериолярный склероз, гломерулярный склероз, атрофия канальцев и интерстициальный фиброз.
Лечение
Лечение направлено на устранение гипокалиемии; клинически значимая гипокалиемия развивается у кошек при концентрации калия в сыворотке крови < 3 ммоль/л.Наиболее безопасным является применение калия перорально, поскольку в таком варианте передозировка практически исключена. Перорально калия глюконат назначается в дозе 2–5 ммоль/день с подбором дозы в зависимости от концентрации калия в крови. Калий в пероральной форме присутствует на рынке в виде препаратов «Аспаркам» и «Панангин», 1 ммоль калия содержится в одной таблетке данных препаратов. При тяжелой гипокалиемии (уровень калия < 1,5 ммоль/л) могут развиваться угрожающие жизни состояния: слабость дыхательной мускулатуры, недостаточная вентиляция легких и даже остановка дыхания. Таким пациентам необходимо срочное размещение в стационаре для внутривенной коррекции гипокалиемии при постоянном контроле уровня калия в сыворотке крови, так как передозировка калия при внутривенном введении может привести с гиперкалиемии и развитию жизнеугрожающих аритмий.
Важным компонентом лечения является препарат «Спиронолактон» – калийсберегающий диуретик, антагонист альдостероновых рецепторов, назначается в дозе 2–4 мг/кг. Действующее вещество препарата связывается с рецепторами альдостерона в клетках дистальных извитых канальцев почек и собирательных трубочек, задерживает калий в организме и способствует натрийурезу. У кошек при использовании данного препарата могут возникать побочные эффекты, такие как анорексия, диарея, рвота и язвенный дерматит. Если применение спиронолактона не обеспечивает достаточного гипотензивного эффекта, который может быть достигнут путем усиленного выведения натрия и воды, рекомендуется рассмотреть назначение амлодипина в дозе 0,625–1,25 мг/кошку каждые 12–24 часа.
При обнаружении новообразования надпочечника(ов) рекомендуется проведение адреналэктомии.
Диагностика заболевания на ранней стадии и своевременное начало лечения позволяют минимизировать повреждение почек. Таким образом, лечение гиперальдостеронизма может рассматриваться как нефропротективная терапия. В случае диагностики вторичного гиперальдостеронизма лечение должно быть направлено на контроль или устранение основного заболевания.
Список литературы:
- Закирова Н. Э., Низамова А. Н. Влияние альдостерона на ремоделирование миокарда у пациентов с хронической сердечной недостаточностью ишемического генеза. Медицинский вестник Башкортостана. Том 16, № 1 (91). – 2021, стр. 5–10.
- Карлович Н. В., Мохорт Т. В., Волчек Ю. А. Ренин-ангиотензин-альдостероновая система: традиционная функция и плейотропные эффекты регуляции фосфорно-кальциевого метаболизма. – Медицинские новости № 10. – 2021, c. 22–25.
- Смирнова О. О. Гиперальдостеронизм кошек. Действительно ли болезнь настолько редка, что не заслуживает нашего внимания? ссылка
- Beate Egner. Feline Endocrine Hypertension. ссылка
- Bento D. Zahn. Feline primary hyperaldosteronism: an emerging endocrine disease. Ciência Rural, Santa Maria, v. 46, n. 4, p. 686–693, Apr 2016.
- Bisignano J. Feline hyperaldosteronism: Recognition and diagnosis. ссылка
- Djajadiningrat-Laanen S., Galac, Boevé М. Evaluation of the oral fludrocortisone suppression test for diagnosing primary hyperaldosteronism in cats. J Vet Intern Med, 27(6): 1493–9, Nov-Dec 2013. doi: 10.1111/jvim.12216.
- Penninck D., d’Andre M. Small Animal Ultrasonography. – Blackwell Publishing Ltd. – 2008. – 502 р.
- Hans S. Primary Hyperaldosteronism in Cats: An Underdiagnosed Disorder.
- Vet Clin North Am Small Anim Pract, 50(5): 1053–1063, Sep 2020.
- Hans S. Primary Hyperaldosteronism in Cats. ссылка
- Tomaschitz А. Aldosterone and parathyroid hormone interactions as mediators of metabolic and cardiovascular disease. Metabolism, 63(1): 20–31, Jan 2014. doi: 10.1016/j.metabol.2013.08.016.
- Vertloo L. Feline Primary Hyperaldosteronism. Reviewed/Revised Jul 2024. ссылка
- Verhoek D. Hyperaldosteronism: The Prevalence and Role in Cats with Chronic Kidney Disease, 2010. ссылка


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург