1ООО «БИОВИЗОР», Москва, Россия.
2Поволжский научно-исследовательский институт производства и переработки мясомолочной продукции, Волгоград, Россия.
3Федеральный научный центр – Всероссийский научно-исследовательский институт экспериментальной ветеринарии имени К. И. Скрябина и Я. Р. Коваленко Российской академии наук, Москва, Россия.
Введение
Паразитарные заболевания широко распространены в России и за рубежом не только у служебных и охотничьих, но и у декоративных пород собак. Чаще всего встречаются токсокароз, дипилидиоз, токсаскаридоз и унцинариоз. Миллионы домашних питомцев загрязняют окружающую среду испражнениями, содержащими возбудителей заболеваний, что создает угрозу заражения для людей и других животных. Быстро увеличивающиеся популяции собак и кошек являются важным фактором биологического загрязнения окружающей среды, особенно в крупных городах и мегаполисах. Во многом это связано с изменением социальной среды и увеличением продолжительности жизни владельцев, которым животные помогают справляться со стрессом и одиночеством. В таких условиях необходимо проводить комплекс профилактических мер, в том числе регулярную дегельминтизацию питомцев1-4.Борьба с гельминтами (нематодами, трематодами, цестодами) представляет собой сложную задачу, поскольку взрослые особи и их личинки могут по-разному реагировать на антипаразитарные препараты. В связи с этим антигельминтные средства могут либо содержать один активный компонент, направленный на уничтожение конкретного класса паразитов, либо являться мультикомпонентными, воздействующими на несколько видов паразитов и/или на разные стадии развития гельминта одновременно5,6.
Учитывая важность расширения ассортимента противопаразитарных лекарственных средств в рамках импортозамещения, компанией ООО «ВИК – здоровье животных» был разработали противопаразитарный препарат «Пинпрамиль».
Оценка биоэквивалентности (фармакокинетической эквивалентности) лекарственных средств является основным видом исследований воспроизведенных (генерических) препаратов, содержащих такое же количество действующего вещества, как в соответствующем оригинальном лекарственном препарате, и позволяет сделать заключение об эффективности и безопасности сравниваемых лекарственных средств на основании меньшего объема доклинических исследований и в более короткие сроки, чем при проведении клинических исследований.
При изучении биоэквивалентности можно оценить скорость и степень всасывания действующих веществ двух сравниваемых препаратов и сделать вывод о биоэквивалентности воспроизведенного препарата в определенной лекарственной форме и дозировке, соответствующих лекарственной форме и дозировке референтного препарата9-12.
В представленной статье описаны и проанализированы результаты изучения биоэквивалентности двух комплексных противопаразитарных препаратов для собак – «Пинпрамиль» (производство ООО «ВИК – здоровье животных», Россия) и «Мильбемакс» (производство Elanco France SAS, Франция). Оба препарата выпускаются в форме таблеток для орального применения и содержат в качестве действующих веществ празиквантел и мильбемицин оксим.
«Мильбемакс» был выбран в качестве референтного препарата на основании данных
электронной системы «Гален» Россельхознадзора, где препарат «Мильбемакс», разработанный компанией Elanco France SAS, имеет действующую регистрацию в Российской Федерации и зарегистрирован на основании результатов доклинических и клинических исследований, подтверждающих его качество, эффективность и безопасность.
Мильбемицин оксим – макроциклический лактон, выделяемый в результате ферментативной деятельности Streptomyces hygroscopicus var. аureolacrimosus, активен в отношении личинок и имаго нематод, паразитирующих в желудочно-кишечном тракте собак, а также в отношении личинок нематоды Dirofilaria immitis. Механизм действия мильбемицина обусловлен повышением проницаемости клеточных мембран для ионов хлора (Cl), что приводит к сверхполяризации мембран клеток нервной и мышечной ткани, параличу и гибели паразита6-8.
Мильбемицина оксим относится к группе макроциклических лактонов, выделяемых в результате ферментации Streptomyces hygroscopkus var. aureolacrimosus, активен в отношении клещей, личиночных и взрослых стадий нематод, а также личинок Dirofilaria immitis. Механизм действия мильбемицина обусловлен повышением проницаемости клеточных мембран для ионов хлора (Cl), что приводит к сверхполяризации мембран клеток нервной и мышечной ткани, параличу и гибели паразита6-8.
Празиквантел является ацилированным производным пиразин-изохинолина, обладает выраженным действием против цестод и нематод, повышает проницаемость клеточных мембран паразита для ионов кальция (Са2+), вызывает деполяризацию мембран, сокращение мускулатуры и разрушение тегумента, что приводит к гибели паразита и способствует его выведению из организма животного. Празиквантел метаболизируется в печени до транс-4-гидроксипразиквантела.
Одновременное использование двух действующих веществ с разным спектром и механизмом противопаразитарного действия в одной лекарственной форме позволило создать универсальный комплексный препарат, который назначают собакам с лечебной и профилактической целью при нематодозах, цестодозах и смешанных нематодо-цестодозных инвазиях.
Цель исследования – сравнение фармакокинетики празиквантела и мильбемицина в крови собак для демонстрации биоэквивалентности (или отсутствия биоэквивалентности) лекарственных препаратов в форме таблеток «Пинпрамиль» (воспроизведенный препарат) и «Мильбемакс» (референтный препарат) при пероральном введении в терапевтической дозировке 1 таблетка, которая содержит 12,5 мг мильбемицина оксима и 125 мг празиквантела.
Материалы и методы
В качестве тест-системы для исследования были выбраны собаки как вид животных, которым в дальнейшем планируется применение препарата, кроме того, им удобно вводить препараты перорально, не нарушая целостность таблеток. Исследование было проведено в 2023 г. на базе приюта для домашних животных, расположенного в Щаповском поселении Троицкого административного округа Москвы. Для работы по принципу аналогов были сформированы две группы собак-метисов (сук и кобелей) в возрасте от 1 до 3 лет, с массой тела 18,8–22,8 кг. Каждая группа животных состояла из 6 особей с индивидуальными номерами. Экспериментальные животные на протяжении не менее 30 суток до начала исследований и в период проведения исследований не получали никаких других лекарственных препаратов.Для экспериментов был применен параллельный дизайн исследований в соответствии с утвержденными правилами (Приказ № 101 Минсельхоза РФ от 6 марта 2018 г.)14, что подразумевало одновременное введение животным одной группы воспроизведенного препарата «Пинпрамиль», собакам второй группы – референтного препарата «Мильбемакс».
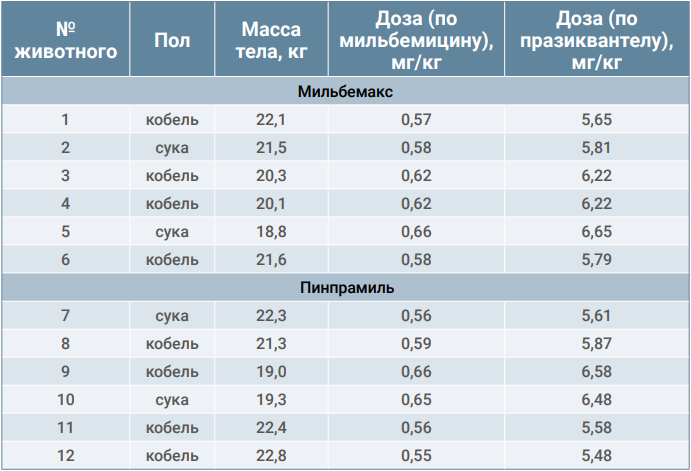
Перед проведением опытов каждое животное взвешивали для расчета индивидуальной дозы препарата. Испытуемые препараты задавали собакам перорально, однократно, индивидуально. В исследовании использовали таблетки «Пинпрамиль» и «Мильбемакс» (в 1 таблетке каждого препарата содержатся эквивалентные количества действующих веществ – 12,5 мг мильбемицина оксима и 125 мг празиквантела). Доза препарата в зависимости от массы тела собаки в соответствии с утвержденной инструкцией референтного препарата составляла 1 таблетку на собаку массой 10–25 кг, что соответствовало от 0,5 до 1,25 мг/кг мильбемицина и от 5,0 до 12,5 мг/кг празиквантела. Индивидуальные значения массы тела экспериментальных собак и полученные ими дозы действующих веществ препаратов в эксперименте представлены в таблице 1.
Временные точки для забора крови у собак выбирали на основании прогнозируемых фармакокинетических профилей действующих веществ: до введения препаратов (0 ч.), через 15, 30, 45 минут и 1, 2, 3, 4, 6, 9, 12, 24, 48, 72, 96 часов после введения препаратов. В каждый срок отбор проб крови был произведен у 6 собак в каждой группе. При проведении манипуляций были соблюдены принципы гуманного обращения с экспериментальными животными, направленные на снижение у них уровня боли и стресса.
Кровь отбирали в одноразовые пробирки с активатором свертывания. После образования сгустка и отделения сыворотки пробы крови центрифугировали при 3500 об/мин в течение 5 минут. После этого сыворотку крови отбирали в пробирки типа Eppendorf (CITOTEST, Китай) в объеме не менее 1 мл, которые замораживали и транспортировали в термоконтейнере в замороженном состоянии в биоаналитическую лабораторию «БИОВИЗОР» (г. Москва).
В ходе исследования определяли концентрации действующих веществ препаратов в сыворотке крови собак. Для этого применяли валидированную методику количественного определения празиквантела, транс-4-гидроксипразиквантела и мильбемицина оксима в экстрактах образцов сыворотки крови животных методом высокоэффективной жидкостной хроматографии с тандемным масс-спектрометрическим детектированием. С этой целью использовали хромато-масс-спектрометр Shimadzu LCMS-8050 (Япония). При валидации методики учитывали следующие показатели: линейность, степень извлечения, специфичность, прецизионность, правильность (точность), пределы количественного и качественного определения, допустимость разбавления, стабильность аналита и внутреннего стандарта.
Полученные концентрации празиквантела, транс-4-гидроксипразиквантела и мильбемицина оксима в сыворотке крови собак использовали для расчета их фармакокинетических параметров: период полувыведения действующего вещества (T1/2), максимальную концентрацию действующего вещества (Cmax), площадь под кривой «концентрация действующего вещества – время» в интервале времени от 0 до момента (t) отбора последней пробы биоматериала (AUC0-t), площадь под кривой «концентрация действующего вещества – время» в интервале времени от 0 до ∞ (AUC0-∞), среднее время удержания вещества в системном кровотоке (MRT), соотношение AUC0-t/AUC0-∞. Значения параметров Cmax, AUC(0-t), AUC(0-∞) послужили основой для оценки биоэквивалентности исследованных препаратов.
Полученные в ходе исследования данные были статистически обработаны, что подразумевало нахождение средних величин, относительных стандартных отклонений от средних и стандартных ошибок в программе Microsoft Excel (США). Фармакокинетические параметры были рассчитаны в программе PKSolver (надстройка для Microsoft Excel) с применением некомпартментной (бескамерной) модели распределения действующих веществ препаратов «Пинпрамиль» и «Мильбемакс» в организме животных.
Результаты и обсуждение
Фармакокинетика празиквантела и транс-4-гидроксипразиквантела в сыворотке крови собак после применения препаратов «Пинпрамиль» и «Мильбемакс»На основании полученных данных было установлено, что празиквантел быстро всасывается из желудочно-кишечного тракта и его обнаруживают в сыворотке крови собак уже спустя 15 минут после введения как воспроизведенного, так и референтного препаратов.
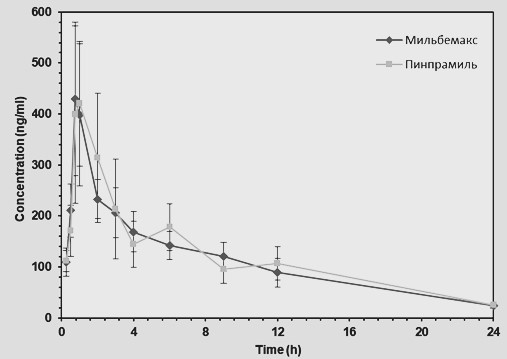
Для воспроизведенного препарата «Пинпрамиль» максимальная концентрация празиквантела в крови была достигнута через 0,75–2 часа после введения и находилась в диапазоне 413,32–607,26 нг/мл. Постепенно в течение двух суток содержание празиквантела в сыворотке крови уменьшалось и через 48 часов было ниже предела количественного определения методики (5 нг/мл).
Похожую картину наблюдали после введения референтного препарата «Мильбемакс»: концентрация празиквантела достигала максимума к 0,75–1 часу после введения и находилась в диапазоне 359,18–594,31 нг/мл. Далее его содержание в сыворотке крови собак постепенно снижалось и к 48 часам также было ниже предела количественного определения методики (5 нг/мл) (НПКО).
Динамика изменения концентрации празиквантела в крови собак представлена на рисунке 1.
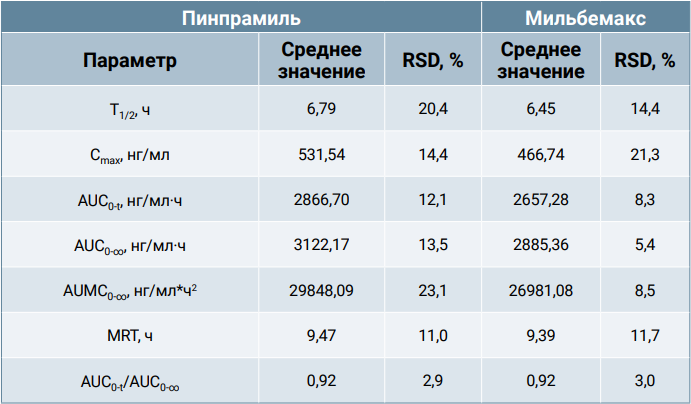
Полученные значения концентрации празиквантела в крови позволили рассчитать его фармакокинетические параметры, которые представлены в таблице 2.
В ходе исследования были получены данные о том, что празиквантел быстро метаболизируется до транс-4-гидроксипразиквантела, который обнаруживают в крови спустя 15 минут после введения препарата.
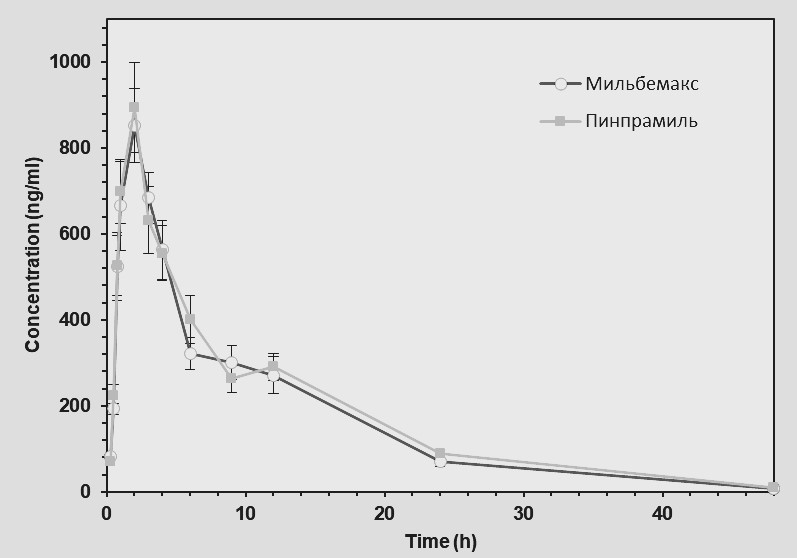
Для воспроизведенного препарата «Пинпрамиль» максимум концентрации транс-4-гидроксипразиквантела в крови был достигнут через 1–3 часа после введения препарата, при этом максимальный его уровень находился в диапазоне 725,56–1171,87 нг/мл. Далее содержание аналита снижалось и к 72 часам не превышало НПКО. В случае референтного препарата «Мильбемакс» уровень транс-4-гидроксипразиквантела также достигал максимума к 1–3 часам после введения препарата и находился в диапазоне 707,31–1046,70 нг/мл. Далее концентрация метаболита в сыворотке крови собак снижалась и к 72 часам не превышала НПКО методики.
Динамика изменения уровня транс-4-гидроксипразиквантела в крови собак представлена на рисунке 2.
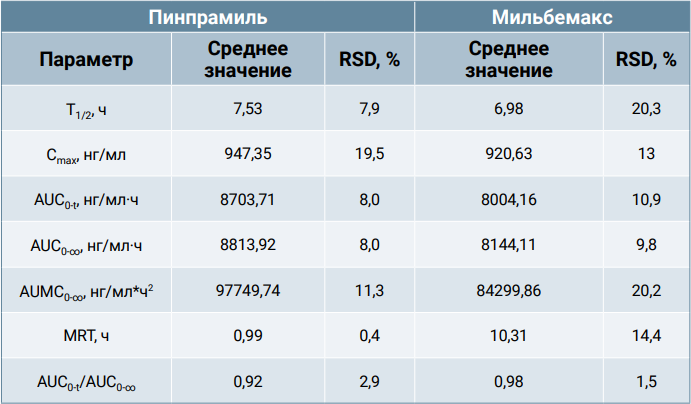
На основании значений концентраций транс-4-гидроксипразиквантела в сыворотке крови собак были рассчитаны его фармакокинетические параметры, которые представлены в таблице 3.
Фармакокинетика мильбемицина оксима в сыворотке крови собак после применения препаратов «Пинпрамиль» и «Мильбемакс»
Полученные данные свидетельствуют о том, что мильбемицин оксим быстро всасывается из желудочно-кишечного тракта и его обнаруживают в сыворотке крови собак спустя 0,25 ч после однократного применения изучаемых препаратов.
Для воспроизведенного препарата «Пинпрамиль» максимум концентрации мильбемицина оксима в крови был достигнут через 1–4 часа после перорального введения, при этом максимальный его уровень находился в диапазоне 146,95–200,10 нг/мл. Постепенно содержание этого аналита в сыворотке крови уменьшалось, но оставалось выше НПКО методики (> 3 нг/мл) даже через 96 часов (4,098–9,583 нг/мл) после ведения препарата.
Схожую картину наблюдали после введения референтного препарата «Мильбемакс»: концентрация мильбемицина оксима достигала максимума к 1–4 часам после введения препарата и находилась в диапазоне 144,498–230,568 нг/мл. Далее уровень этого аналита снижался и к 96 часам находился в диапазоне от 5,299 до 11,381 нг/мл.
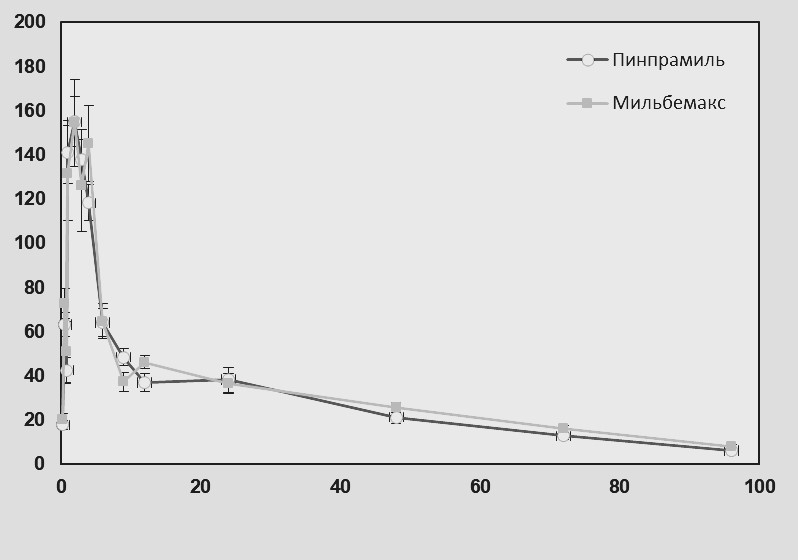
Сравнительная динамика изменения концентрации мильбемицина оксима в крови собак представлена на рисунке 3.
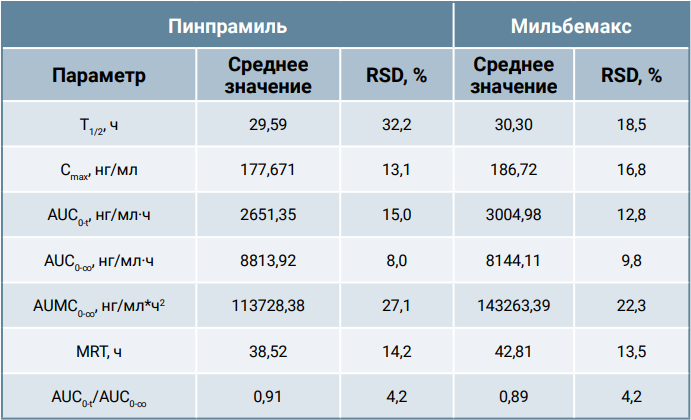
Фармакокинетические параметры мильбемицина оксима, которые были рассчитаны на основе полученных значений его концентраций в сыворотке крови собак, представлены в таблице 4.
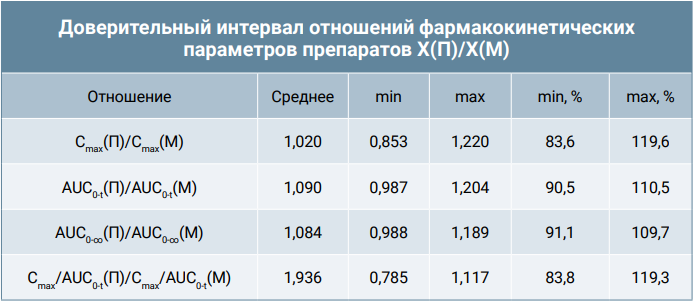
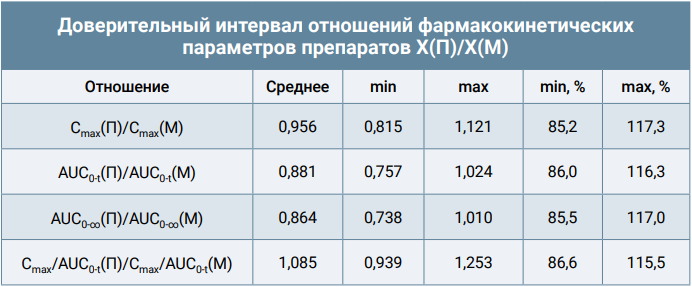
Наличие/отсутствие биоэквивалентности между воспроизведенным препаратом «Пинпрамиль» и референтным препаратом «Мильбемакс», отобранным для исследований по лекарственной форме и содержанию действующих веществ, оценивали в соответствии с Правилами проведения исследований биоэквивалентности лекарственных средств Евразийского экономического союза (решение совета ЕЭК № 85 от 15.02.2023 г.). Биоэквивалентность препаратов оценивали на основании предположения о логнормальном распределении измеренных величин Cmax, AUC(0-t), AUC(0-∞) и Cmax/AUC(0-t).
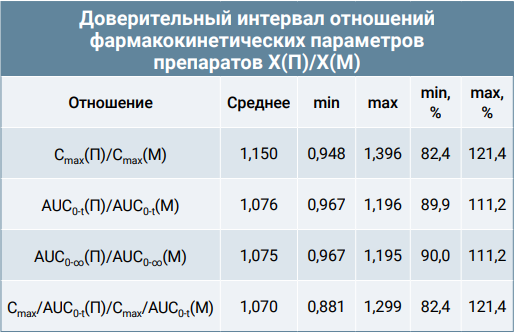
Результаты расчета доверительных интервалов для отношений фармакокинетических параметров действующих веществ представлены в таблицах 5-7.
Для празиквантела, транс-4-гидроксипразиквантела и мильбемицина оксима двусторонние доверительные интервалы для отношений Cmax, AUC0-t, AUC0-∞ находились в пределах 80–125%, а для отношений Cmax/AUC0-t – в пределах 75–133%. Таким образом, проведенное исследование показало, что препараты «Мильбемакс» и «Пинпрамиль» являются биоэквивалентными.
Выводы
Результаты изучения сравнительной фармакокинетики воспроизведенного препарата «Пинпрамиль» и референтного препарата «Мильбемакс» в организме собак продемонстрировали их фармацевтическую эквивалентность с учетом того, что двусторонние доверительные интервалы для отношений Cmax, AUC0-t, AUC0-∞ находились в диапазоне 80–125%, а отношений Cmax/AUC0-t – в диапазоне 75–133%.Биофармацевтические свойства препарата «Пинпрамиль» сопоставимы с аналогичными свойствами препарата «Мильбемакс», который ранее был зарегистрирован в РФ, на основании результатов доклинических и клинических исследований, подтвердивших его качество, эффективность и безопасность.
Таким образом, полученные результаты свидетельствуют о том, что разработанный в рамках импортозамещения отечественный препарат «Пинпрамиль» обладает аналогичной с референтным препаратом безопасностью и терапевтической эффективностью, что позволяет рекомендовать его для лечения и профилактики гельминтозов собак.
Авторы объявили об отсутствии конфликта интересов.
Список литературы:
- Тимербаева Р.Р., Бектемирова М.Р., Латыпов Д.Г. Гельминтозы плотоядных животных советского района г. Казани. Ученые записки казанской государственной академии ветеринарной медицины им. Н.Э. Баумана. 2018; 4 (236); 186-190. DOI: 10.31588/2413-4201-1883-236-4-186-190. EDN: PJTYRP.
- Линовицкая А. А., Сайтханов Э. О., Концевая С. Ю. Зоонозы плотоядных животных и человека на территории города Коломна московской области. Исследование эффективности препарата Мильбемакс. Вестник рязанского государственного агротехнологического университета им. П.А. Костычева. 2019; 1(41); 44-51. EDN: DLRQPG.
- Виолин Б. В., Верещагина Д.А. Терапевтическая эффективность применения антигельминтного препарата на основе мебендазола/празиквантела для лечения гельминтозов собак. Ветеринарный врач. 2006; 2; 32-33. EDN JXCQY.
- Rebecca J. Traub, Patsy A. Zendejas-Heredia, Luca Massetti, Vito Colella. Zoonotic hookworms of dogs and cats – lessons from the past to inform current knowledge and future directions of research. International Journal for Parasitology. V. 51, Iss. 13–14, December 2021, P. 1233-1241
- Поносов С. В., Попцова С. В. Применение различных комплексных антигельминтных препаратов для собак. Известия Оренбургского государственного аграрного университета. 2019; 6(80); 226-228. EDN CTERHE.
- В. А. Оробец, О. И. Севостьянова, И. В. Заиченко [и др.]. Эффективность нового антигельминтного препарата Supramil® таблетки при кишечных гельминтозах собак и кошек. Российский ветеринарный журнал. 2022; 2; 30-41. DOI 10.32416/2500-4379-2022-2-30-41. EDN WUNDAJ.
- Арисов М. В., Абрамов В. Е., Балышев А. В., Демин А. И. Особенности фармакокинетики действующих веществ препарата "Гельминтал" (сироп). Ветеринария, зоотехния и биотехнология. 2016; 12; 43-47. EDN XIKEBX.
- Оробец, В. А., Мукасеев С. В., Зейналов О. А. Токсикологическая оценка антигельминтного препарата Supramil® таблетки для собак и кошек. Ветеринария. 2022; 6; 55-62. DOI 10.30896/0042-4846.2022.25.6.55-62. EDN EARXJY.
- Шинкаренко А. Н., Каменов К. С., Мукасеев С. В., Зейналов О. А. Оценка эффективности нового антигельминтного препарата Supramil® таблетки для профилактики дирофиляриоза собак. Российский ветеринарный журнал. 2022; 3-4; 31-35. DOI 10.32416/2500-4379-2022-3-4-31-35. EDN SWYPVL.
- Понамарев В.С., Лунегов А.М. Релевантные дизайны исследования на биоэквивалентность лекарственных средств для ветеринарного применения. Вопросы нормативно-правового регулирования в ветеринарии. 2021; 2: 81-84. DOI 10.17238/issn2072-6023.2021.2.81. EDN LRGXHY.
- Понамарев, В. С. Менеджмент качества при оценке биоэквивалентности: проблемы и перспективы. Нормативно-правовое регулирование в ветеринарии. 2022; 2; 98-101. DOI 10.52419/issn2782-6252.2022.2.98. EDN EBOKSD.
- Давыдова К. С., Шохин И. Е., Раменская Г. В., Кукес В. Г. Подходы к оценке эквивалентности воспроизведенных лекарственных средств в современной фармацевтической практике. Вестник фармации. 2010; 3(63); 66-68. EDN TXUNSB.
- А. В. Соколов, В. Г. Кукес, Н. Д. Бунятян [и др.]. Фармакокинетический подход в вопросе о взаимозаменяемости лекарственных средств. Биомедицина. 2015; 3; 43-51. EDN VCTPED.
- Приказ Минсельхоза РФ от 6 марта 2018 г. № 101 «Об утверждении правил проведения доклинического исследования лекарственного средства для ветеринарного применения, клинического исследования лекарственного препарата для ветеринарного применения.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург