Резюме
Актуальность. Гемангиосаркома (ГСА) селезенки у собак представляет собой злокачественное высокоагрессивное опухолевое заболевание с ранним метастазированием. Гемангиосаркома поражает преимущественно породы собак средних, крупных и гигантских размеров, а также их метисов. Стандартом лечения ГСА селезенки является спленэктомия с последующей адъювантной химиотерапией, однако прогноз остается осторожным, несмотря на проводимое лечение. Липосомальный доксорубицин (ЛД), обладающий способностью к селективному накоплению в опухолевой ткани и сниженной кардиотоксичностью, представляет интерес в лечении диссеминированных форм ГСА.Цель. Предоставить описание клинического случая применения ЛД у собаки с метастатической ГСА селезенки, оценить его эффективность и безопасность ЛД в сравнении со стандартным доксорубицином, включенным в комплексный противоопухолевый протокол VAC.
Материалы и методы. Собаке породы метис (10 лет) с диагностированной после спленэктомии ГСА с метастазами в печень была назначена противоопухолевая химиотерапия. Первоначально был назначен протокол VAC (винкристин, доксорубицин, циклофосфамид), однако из-за развития тяжелых осложнений на фоне применения доксорубицина (септицемия, панкреатит, острая почечная недостаточность) данный протокол был прекращен. После стабилизации состояния пациента была начата монотерапия липосомальным доксорубицином (ЛД) в дозе 30 мг/м2 внутривенно каждые 3 недели. Мониторинг состояния собаки включал ультразвуковое исследование органов брюшной полости, компьютерную томографию (КТ), общий и биохимический анализы крови, исследование крови на тропонин, эхокардиографию.
Результаты. На фоне терапии липосомальным доксорубицином была достигнута положительная динамика. По данным КТ, проведенной спустя 78 дней после начала лечения, наблюдалось уменьшение объема и количества метастатических очагов в печени по сравнению с предыдущим исследованием.
Общая выживаемость пациента с момента постановки диагноза составила 388 дней. Среди побочных эффектов терапии ЛД наблюдались ладонно-подошвенный синдром (ЛПС), или пальмоплантарная эритродизестезия (ППЭ), купированная снижением дозы до 25 мг/м2, и транзиторная лейкопения I степени, которая не требовала дополнительных лечебных мероприятий. Признаков кардиотоксичности в течение всего периода лечения и последующего наблюдения не было выявлено.
Заключение. Применение липосомального доксорубицина в описанном клиническом случае продемонстрировало эффективность и лучшую переносимость по сравнению с использованием нативного доксорубицина, после которого были зафиксированы тяжелые системные осложнения. ЛД может рассматриваться как перспективный вариант терапии метастатической ГСА, особенно у пациентов с повышенным риском осложнений желудочно-кишечного тракта и кардиотоксичности.
Введение
Гемангиосаркома (ГСА) – злокачественная опухоль, происходящая из эндотелиальных клеток кровеносных сосудов. У собак она составляет около 2% всех опухолей и от 45 до 51% всех злокачественных новообразований селезенки1,2. Данному заболеванию более подвержены собаки среднего и пожилого возраста, а также представители таких пород, как немецкая овчарка, доберман, ротвейлер, немецкий дог, золотистый ретривер и лабрадор-ретривер3.ГСА селезенки характеризуется агрессивным течением и ранним гематогенным метастазированием, чаще всего в печень и легкие. Золотым стандартом лечения является спленэктомия, однако без последующей адъювантной химиотерапии медиана выживаемости редко превышает 1–3 месяца4. Традиционные протоколы, включающие доксорубицин в комбинации с циклофосфамидом, позволяют увеличить медиану выживаемости до 6–9 месяцев, но сопряжены с риском развития миелосупрессии, гастроинтестинальной токсичности и кардиотоксичности5.
Липосомальная форма доксорубицина обладает измененной фармакокинетикой: за счет эффекта усиленной проницаемости и удержания (EPR-effect) она селективно накапливается в опухолевой ткани, что потенциально повышает ее эффективность и снижает системную токсичность, в частности риск развития кардиомиопатии6.
Целью данной статьи является описание клинического случая успешного применения липосомального доксорубицина у собаки с метастатической ГСА селезенки после развития тяжелых осложнений на фоне стандартного химиотерапевтического протокола13,14.
Клинический случай
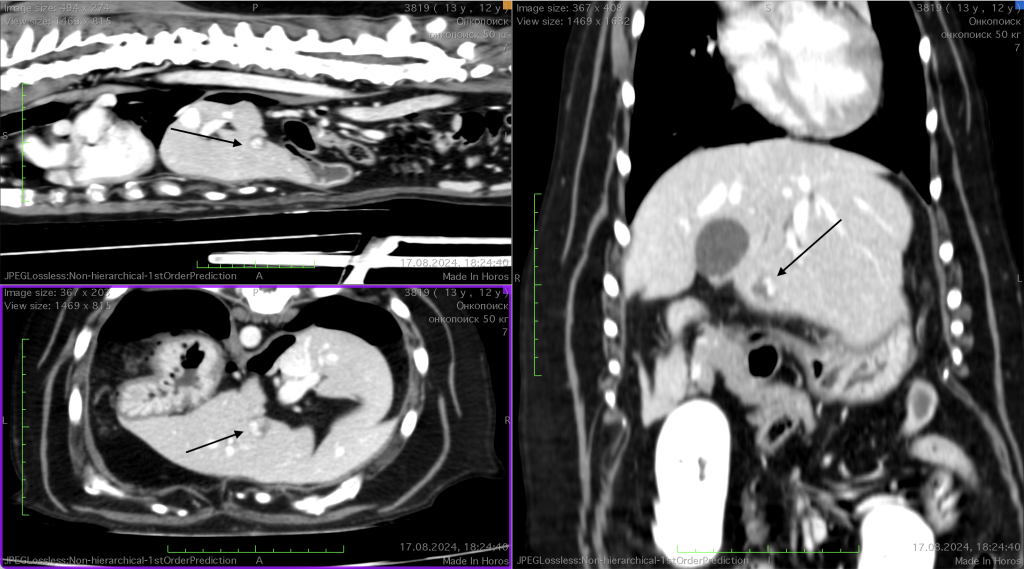
Анамнез и диагностика. У собаки (метис, 10 лет, интактный кобель) в ходе планового обследования во время проведения УЗИ было выявлено бессимптомное новообразование селезенки. При динамическом наблюдении за состоянием пациента в течение месяца был зафиксирован выраженный рост новообразования. В связи с этим 03.08.2024 было принято решение о проведении компьютерно-томографического исследования с ангиографией. Исследование подтвердило наличие новообразования селезенки, характеризующегося гетерогенным накоплением контраста (фото 1.1), а также множественных гиперваскуляризированных участков в тканях селезенки. На основании полученных данных было принято решение о выполнении спленэктомии по стандартной методике.17.08.2024 после получения гистологического заключения, подтверждающего диагноз «гемангиосаркома селезенки», была проведена контрольная компьютерная томография. На данном этапе исследования в печени были обнаружены единичные очаги, подозрительные в отношении метастатических очагов (фото 1.2).
Лечение и динамика
- 19.08.2024 была начата адъювантная противоопухолевая терапия по протоколу VAC (винкристин, доксорубицин, циклофосфамид). После первого введения доксорубицина в дозе 30 мг/м2 и последующих препаратов у животного развились тяжелый диспептический синдром, септицемия и острая почечная недостаточность (ОПН), что потребовало отмены противоопухолевой терапии, стабилизации состояния и интенсивного лечения.
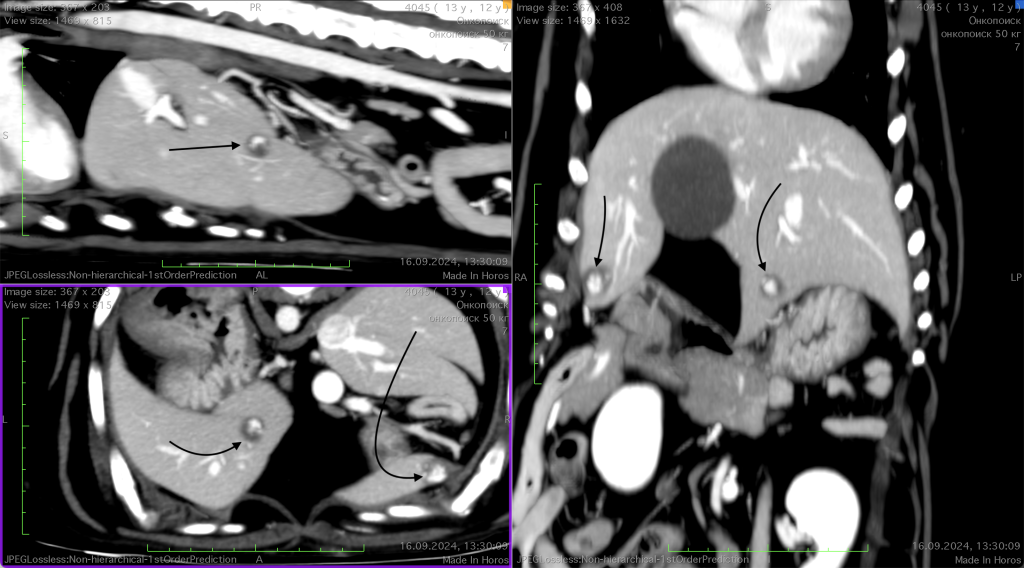
- 16.09.2024 после клинического улучшения состояния пациента была проведена контрольная КТ, которая показала отсутствие прогрессирования метастатических очагов в печени на фоне прекращения лечения (рис. 2, 3).
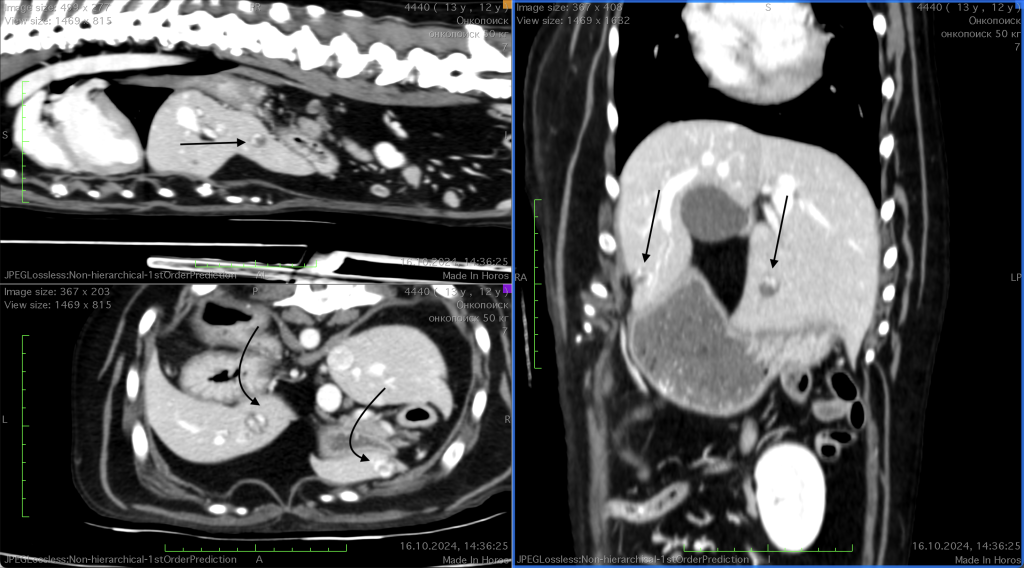
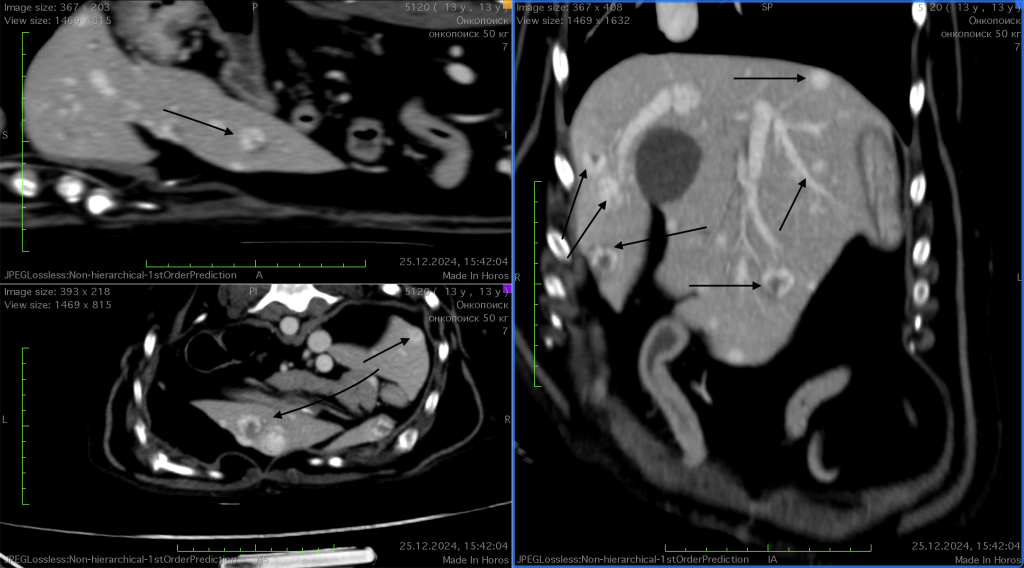
На фоне отмены доксорубицина и вынужденного отказа от протокола VAC, КТ от 25.12.2024 показала отрицательную динамику: увеличение объема и количества метастатических очагов в печени (фото 4).
Второй этап противоопухолевой химиотерапии (липосомальный доксорубицин)
В связи с прогрессированием основного заболевания и непереносимостью стандартного протокола 12.01.2025 была начата монотерапия липосомальным доксорубицином (ЛД) в дозе 30 мг/м2 внутривенно каждые 3 недели. Перед каждым введением проводился контроль анализов крови – общий клинический анализ крови, биохимический анализ крови, анализ уровня тропонина.
Результаты
Ответ на лечение
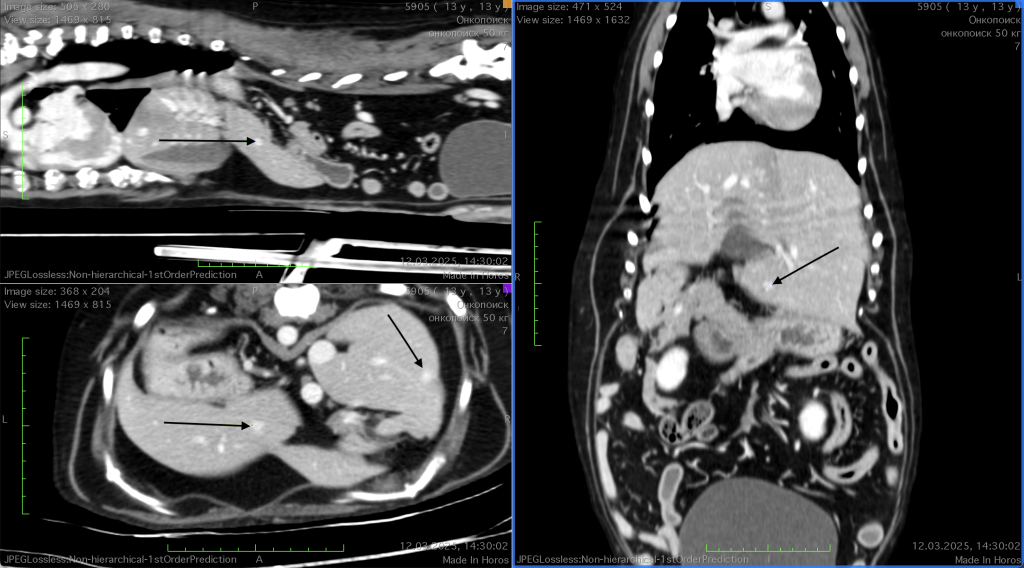
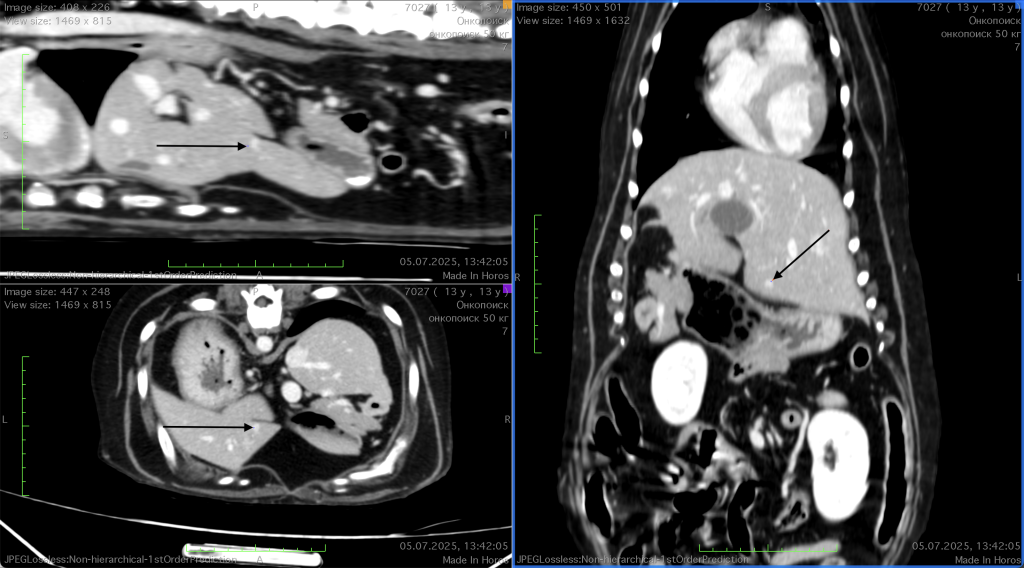
Контрольное КТ-исследование, проведенное 12.03.2025 после двух введений ЛД (фото 5), продемонстрировало выраженную положительную динамику: в печени наблюдалось уменьшение объема и количества метастатических очагов по сравнению с результатами предыдущего исследования от 25.12.2024 (фото 4).Таким образом, было документально подтверждено начало частичной ремиссии на фоне терапии, которая поддерживалась за счет регулярных (каждый 21 день) введений ЛД, что также было подтверждено контрольным КТ-исследованием, проведенным 05.07.2025 (фото 6).
Побочные эффекты и их коррекция
Ладонно-подошвенный синдром (ЛПС)
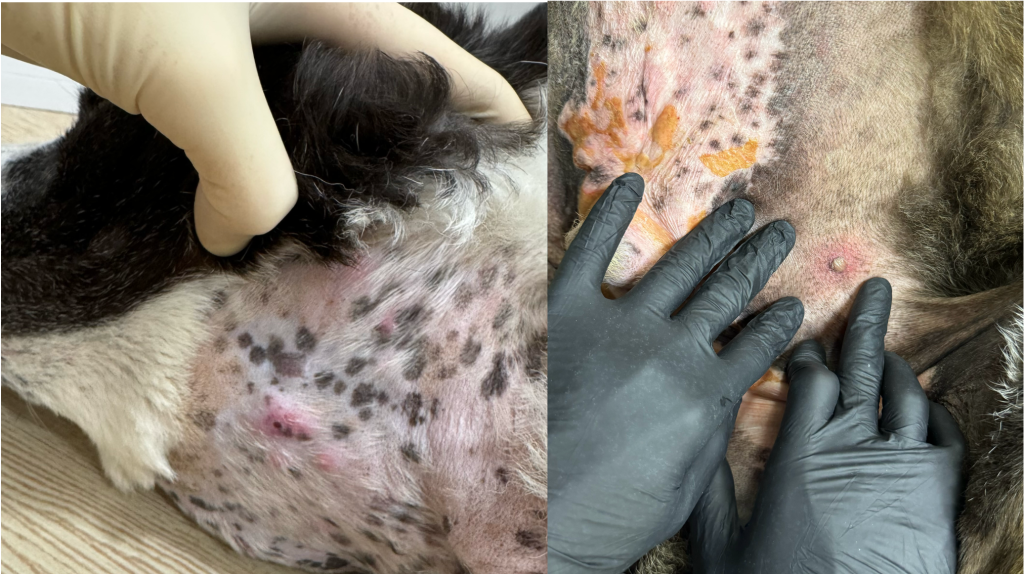
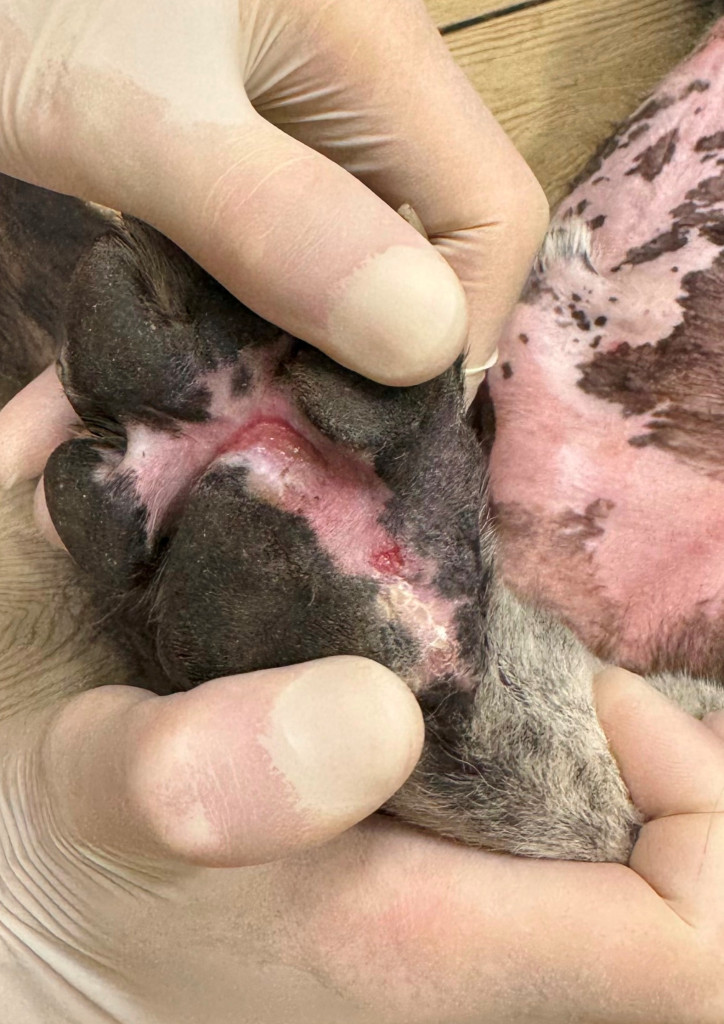
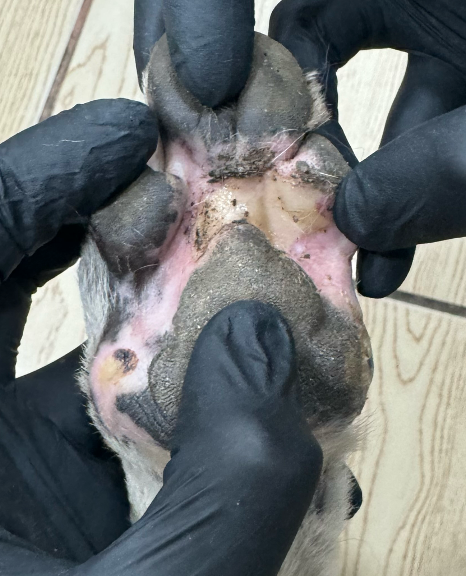
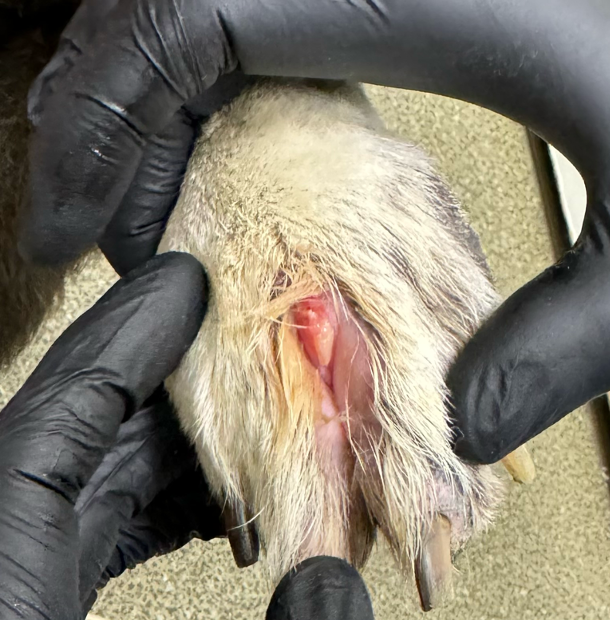
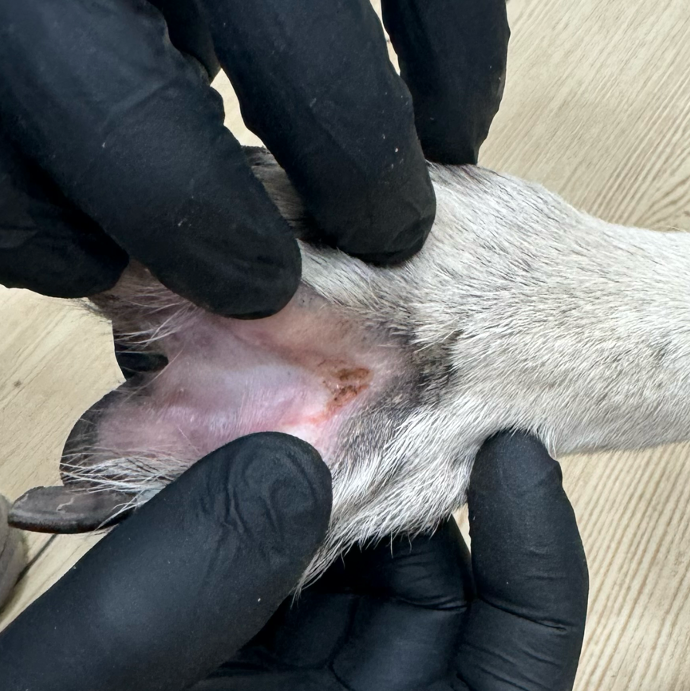
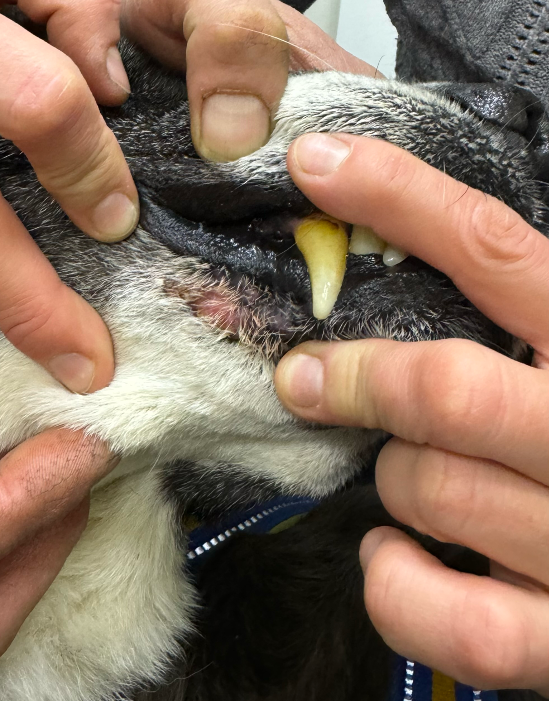
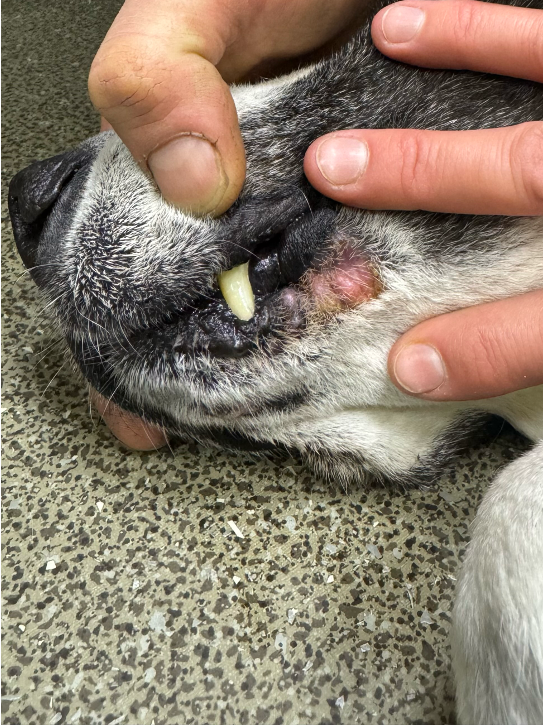
После первого и второго введения ЛД у собаки развился кожный синдром, характеризующийся эритемой и шелушением в области подмышечных впадин, вентральной поверхности живота (фото 7), шеи и паха (фото 7, 8). Данное осложнение известно как характерное для применения ЛД8. После снижения дозы ЛД до 25 мг/м2 выраженность ЛПС заметно снизилась, что позволило продолжить терапию.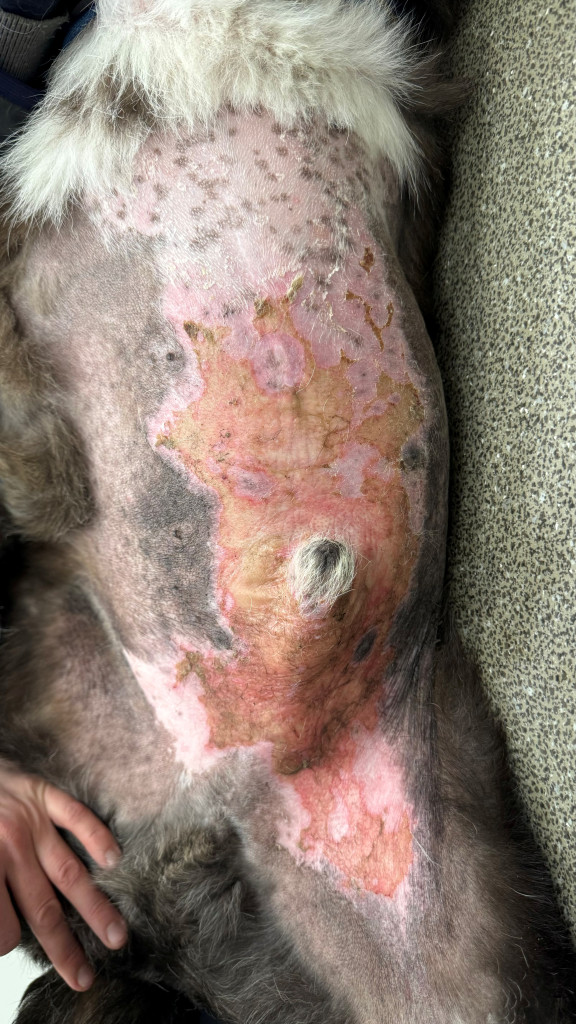 Фото 7.1 Эритродизестезия на фоне введенного липосомального доксорубицина с положительной динамикой.
Фото 7.1 Эритродизестезия на фоне введенного липосомального доксорубицина с положительной динамикой.
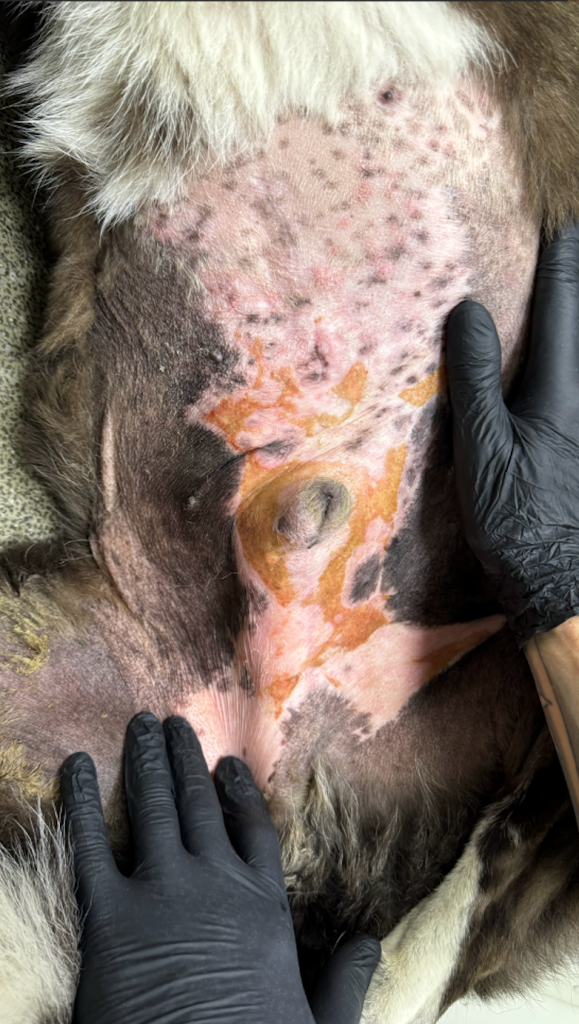 Фото 7.2 Эритродизестезия на фоне введенного липосомального доксорубицина с положительной динамикой.
Фото 7.2 Эритродизестезия на фоне введенного липосомального доксорубицина с положительной динамикой.
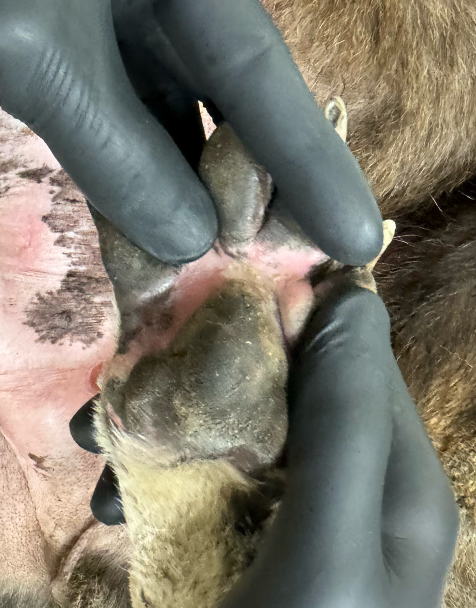
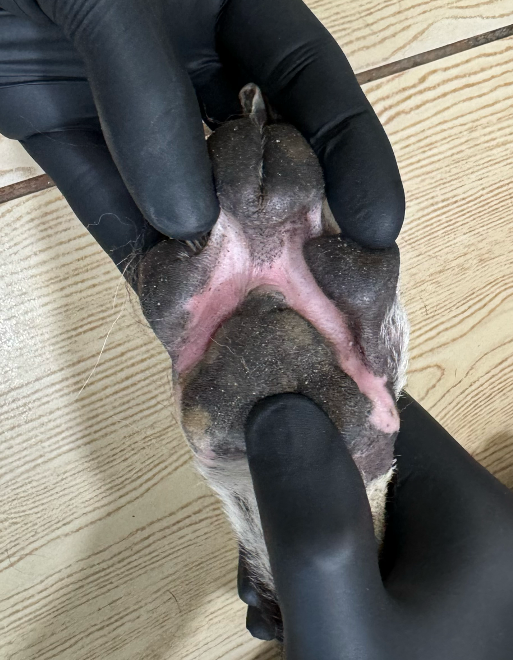
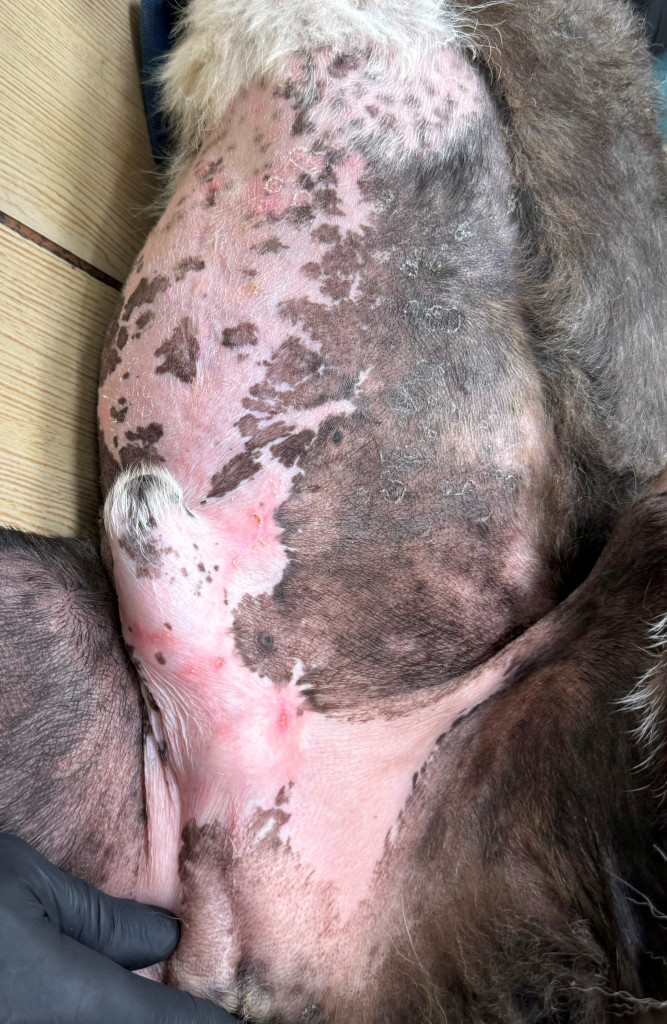 Фото 7.3 Эритродизестезия на фоне введенного липосомального доксорубицина с положительной динамикой.
Фото 7.3 Эритродизестезия на фоне введенного липосомального доксорубицина с положительной динамикой.
Ладонно-подошвенный синдром (ЛПС), или пальмоплантарная эритродизестезия (ППЭ), – это характерная и достаточно распространенная дерматологическая токсическая реакция, ассоциированная с приемом некоторых химиотерапевтических препаратов7. Впервые данный синдром был описан в 1984 году Локичем и Муром (Lokich J. J., Moore C.) из госпиталя New England Deaconess Hospital8 при проведении непрерывной инфузии 5-фторурацила (5-ФУ). В дальнейшем ЛПС/ППЭ была связана с действием целого ряда других препаратов, включая пегилированный липосомальный доксорубицин (ПЛД), доксорубицин в режиме непрерывной инфузии, цитарабин, флоксуридин, высокие дозы интерлейкина-2, доцетаксел, капецитабин, винорелбин и гемцитабин7,10.
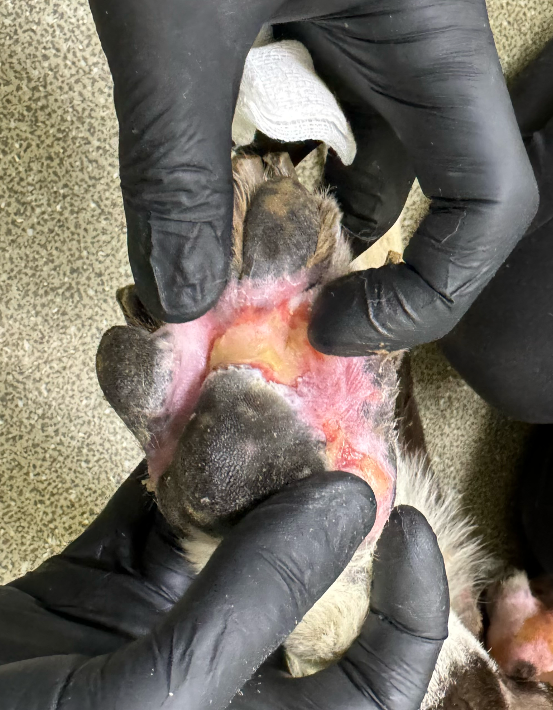
Клиническая картина ЛПС/ППЭ обычно начинается с дизестезии, которая может проявляться в виде хромоты, разлизывания дистальных отделов конечностей. Симптомы могут возникнуть через 2–12 дней после введения липосомального доксорубицина. В течение последующих 3–4 дней они часто прогрессируют до симметричного отека и эритемы на подошвенных поверхностях грудных и тазовых конечностей (фото 9). На участках, подверженных давлению, появляются эритематозные бляшки с фиолетовым оттенком и отечные пятна. При легком течении эти проявления самостоятельно разрешаются спустя 1–2 недели (фото 9-11). Однако, если следующий цикл химиотерапии не отложить или не снизить дозу препарата, ЛПС/ППЭ может прогрессировать до буллезной десквамации, образования корок, изъязвления и даже некроза эпидермиса. Подобные осложнения могут быть выраженными и существенно ограничивать повседневную активность пациентов14.
Дополнительно могут поражаться паховая область, мошонка и губы (фото 7, 8, 12).
Гематологическая токсичность
Отмечалась транзиторная лейкопения I степени, не требующая коррекции назначенного лечения.
Кардиотоксичность
При проведении эхокардиографии на фоне терапии ЛД признаков доксорубицин-индуцированной кардиомиопатии не было выявлено. Это согласуется с литературными данными9, указывающими на сниженную кардиотоксичность ЛД по сравнению со свободной формой препарата, особенно при кумулятивных дозах ниже 240 мг/м2.
Гастроинтестинальные осложнения и септицемия
Важно отметить, что в отличие от стандартного доксорубицина при применении ЛД не наблюдались тяжелые гастроинтестинальные осложнения (рвота, диарея, панкреатит) или септицемия.
Выживаемость. С момента постановки диагноза (03.08.2024) общая выживаемость составила 388 дней. Период до прогрессирования заболевания (PFS) на фоне лечения ЛД составил не менее 90 дней, начиная с 12.01.2025 и продолжаясь до 12.03.2025. В течение этого периода времени зафиксировано документально подтвержденное уменьшение размеров метастатических поражений. Смерть наступила вследствие причин, не связанных с основным заболеванием, на фоне полной клинической ремиссии основного заболевания.
Обсуждение
Представленный клинический случай демонстрирует сложность лечения метастатической ГСА и важность индивидуального подбора терапии. Первоначальная попытка применения агрессивного протокола VAC привела к развитию угрожающих жизни осложнений (септицемия, ОПН), что вынудило отказаться от его использования. Несмотря на это, удалось достичь периода стабилизации, после которого было отмечено прогрессирование заболевания.Последующее применение липосомального доксорубицина позволило не только добиться контроля над заболеванием (документально подтвержденный регресс метастазов в печени), но и избежать тяжелых системных осложнений, наблюдавшихся при использовании стандартного доксорубицина. Ключевым преимуществом ЛД в данном случае стал его улучшенный профиль безопасности, что особенно критично для пациента, уже перенесшего осложнения.
Основным побочным эффектом ЛД явился ладонно-подошвенный синдром (ЛПС/ППЭ), который успешно контролировался путем снижения дозы препарата без потери его терапевтической эффективности. Отсутствие признаков кардиотоксичности также является важным преимуществом для собак пожилого возраста, находящихся в основной группе риска по ГСА1-4,12.
Кроме того, стоит отметить, что результаты исследований, направленных на оценку эффективности и токсичности пегилированного липосомального доксорубицина у собак с гемангиосаркомой селезенки, демонстрируют отсутствие статистически значимой разницы в общей медиане выживаемости при сравнении с применением нативного доксорубицина.
Липосомальный доксорубицин в данном клиническом случае рассматривался как препарат с потенциально менее выраженными осложнениями со стороны желудочно-кишечного тракта и меньшей кардиотоксичностью по сравнению с нативным доксорубицином как у людей, так и у собак13,14. Недавнее исследование подтвердило, что ЛД значительно эффективнее подавляет миграцию клеток метастатической остеосаркомы у собак, чем обычный доксорубицин (разница статистически значима, P ≤ 0,05). В эксперименте на куриных эмбрионах (ex ovo) оба препарата показали сходное действие на опухолевые клетки. Однако для окончательного подтверждения эффективности липосомального доксорубицина необходимы дальнейшие исследования на живых организмах (in vivo)15. Также положительный эффект и безопасность применения ЛД были отмечены в медицинском многоцентровом исследовании, где препарат использовался для лечения пациентов с Т-клеточной лимфомой кожи16.
Вывод: таким образом, липосомальная форма доксорубицина является перспективным средством для лечения не только запущенных форм гемангиосарком, но и других форм диссеминированных системных и метастатических заболеваний мелких домашних животных.
Заключение
Применение липосомального доксорубицина в адъювантном режиме у собаки с метастатической гемангиосаркомой селезенки продемонстрировало клиническую эффективность и значительно лучшую переносимость по сравнению со стандартным химиотерапевтическим протоколом. В случаях, когда применение химиотерапии невозможно из-за развития тяжелых побочных эффектов, ЛД представляет собой ценный альтернативный вариант, позволяющий добиться контроля над заболеванием и продлить жизнь пациента при сохранении удовлетворительного качества жизни.Список литературы:
- Spangler W. L., Culbertson M. R. Prevalence, type, and importance of splenic diseases in dogs: 1480 cases (1985-1989). J Am Vet Med Assoc, 200:829–834, 1992.
- Prymak C., McKee L. J., Goldschmidt M. H., et al. Epidemiologic, clinical, pathologic, and prognostic characteristics of splenic hem- angiosarcoma and splenic hematoma in dogs: 217 cases (1985). J Am Vet Med Assoc, 193:706–712, 1988.
- Brown N. O., Patnaik A. K., MacEwen E. G. Canine hemangiosarcoma: retrospective analysis of 104 cases. J Am Vet Med Assoc, 186:56–58, 1985.
- Clifford C. A., de Lorimier L. P. Hemangiosarcoma. In Ettinger S. J., Feldman E. C., Cote E., editors. Textbook of veterinary internal medicine, 8th ed, pp 2093–2102, 2017.
- Spangler W. L., Kass P. H. Pathologic factors affecting postsplenec-tomy survival in dogs. J Vet Intern Med, 11:166–171, 1997.
- Schultheiss P. C. A retrospective study of visceral and nonvisceral hemangiosarcoma and hemangiomas in domestic animals. J Vet.Diagn Invest, 16:522–526, 2004.
- Nagore E., Insa A., Sanmartin O. Antineoplastic therapy-induced palmar plantar erythrodysesthesia (‘hand-foot’) syndrome: incidence, recognition and management. Am J Clin Dermatol, 1:225–234, 2000.
- Lokich J. J., Moore C. Chemotherapy-associated palmar-plantar erythrodysesthesia syndrome. Ann Intern Med, 101:798–799, 1984.
- Comandone A., Bretti S., La Grotta G. Palmar-plantar erythrodysestasia syndrome associated with 5-fluorouracil treatment. Anticancer Res, 13:1781–1783, 1993.
- Jacobi U., Waibler E., Schulze P. Release of doxorubicin in sweat: first step to induce the palmar-plantar erythrodysesthesia syndrome. Ann Oncol, 16:1210–1211, 2005.
- Robert M. Rifkin, et al. Pegylated liposomal doxorubicin, vincristine, and dexamethasone provide significant reduction in toxicity compared with doxorubicin, vincristine, and dexamethasone in patients with newly diagnosed multiple myeloma: a phase III multicenter randomized trial. Cancer. 106:848–858, 2006.
- Mullin C., Clifford C. A. Miscellaneous tumours: Hemangiosarcoma. In: Withrow S. J., Vail D. M., Page R. L., editors. Withrow and MacEwen’s Small Animal Clinical Oncology. 5th ed, pp. 773–778, 2020.
- Working P. K., Newman M. S., et al. Reduction of the cardiotoxicity of doxorubicin in rabbits and dogs by encapsulation in long-circulating, pegylated liposomes. The Journal of Pharmacology and Experimental Therapeutics, 289:1128–1133, 1999.
- Teske E., Rutteman G., et al. A randomized controlled study into the efficacy and toxicity of pegylated liposome encapsulated doxorubicin as an adjuvant therapy in dogs with splenic haemangiosarcoma. Vet Comp Oncol, 9(4):283–9, Dec 2011.
- Magdalena Walewska, Anna Małek, Bartosz Taciak, et al. PEG-liposomal doxorubicin as a potential agent for canine metastatic osteosarcoma – in vitro and ex ovo studies, 2023.
- Uwe Wollina, Reinhard Dummer, Norbert H. Brockmeyer, et al. Multicenter study of pegylated liposomal doxorubicin in patients with cutaneous T-cell lymphoma, 2003.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург