Аннотация
В данной статье представлен клинический случай карциномы поджелудочной железы у кошки. Описаны клинические проявления, включая гипорексию и хроническую рвоту непереваренным кормом, наблюдавшиеся на протяжении шести месяцев. В результатах общего и биохимического анализов крови значимых отклонений не отмечалось. При ультразвуковом исследовании было обнаружено объемное образование в проекции тела поджелудочной железы размером 5,5×5,0 см, неоднородное по структуре и эхогенности. Окончательный диагноз был поставлен на основании гистологического исследования.Насколько известно автору статьи, карцинома поджелудочной железы у кошек является редким заболеванием.
Ключевые слова: карцинома, диагностическая лапаротомия, биопсия, кошка.
Карцинома поджелудочной железы – это редкая опухоль ацинарных клеток или протоков поджелудочной железы у кошек1,2. Этиология данной патологии остается недостаточно изученной и вызывает дискуссии среди специалистов в области онкологии. Опухоль характеризуется высокой степенью метастазирования и агрессивным течением. Прогноз для кошек с карциномой поджелудочной железы неблагоприятный, что обусловлено выраженной инвазивностью и ранним метастазированием, приводящим к срокам выживаемости от нескольких дней до нескольких недель3,4. Метастазы чаще всего локализуются в регионарных лимфатических узлах, печени, селезенке, а также могут поражать почки, диафрагму, плевру, легкие и сердце. В некоторых случаях наблюдается абдоминальный канцероматоз1-5. Средний возраст кошек на момент обнаружения опухоли и постановки диагноза составляет от 11,0 до 11,6 лет3,4. Породная и половая предрасположенность к развитию данной патологии не выявлена.
Клинические признаки неспецифичны и могут быть схожи с симптомами других заболеваний желудочно-кишечного тракта; наиболее часто встречаются гипорексия, вплоть до анорексии, потеря веса, хроническая рвота и диарея. Согласно данным зарубежной литературы, у пациентов с сахарным диабетом наблюдается повышенная частота развития карциномы поджелудочной железы, что, в свою очередь, открывает возможности для дальнейшего изучения механизма развития данного заболевания4,5. Кроме того, среди сопутствующих заболеваний у пациентов с новообразованиями поджелудочной железы часто наблюдаются хроническая болезнь почек, хронический панкреатит, алиментарная лимфома и бронхопневмония.
При физикальном осмотре на первичном приеме (без использования дополнительных методов диагностики) методом пальпации можно выявить образование в эпигастральной области3-6.
Обнаружение у пациента абдоминального выпота (метастатический выпот) при проведении дополнительной диагностики является отрицательным прогностическим индикатором выживаемости.
В литературе имеются данные о том, что комбинированное применение хирургического вмешательства и химиотерапии способствует увеличению продолжительности жизни пациентов. Однако, несмотря на это, не более 10% кошек живут дольше 1 года. У пациентов, не подвергавшихся хирургическому лечению, химиотерапии или лучевой терапии, среднее время выживаемости после выявления новообразования при поддерживающей терапии составляет от 3 до 90 дней5.
Специфических изменений в клиническом и биохимическом анализах крови не отмечается, иногда у пациентов можно выявить нейтропению, нерегенераторную анемию. Повышение ионизированного кальция в крови – плохой прогностический признак, поскольку он зачастую является маркером паранеопластического синдрома.
Конкретные протоколы химиотерапии для пациентов с карциномой поджелудочной железы не установлены из-за редкости и в целом неблагоприятного прогноза этой опухоли.
В зарубежной литературе (Andrea Dedeaux, et al.; 2018) упоминается лечение 11-летней кошки с диагностированной карциномой поджелудочной железы тоцераниба фосфатом (Palladia, Zoetis) в дозе 2,5 мг/кг, перорально, 3 раза в неделю. Через 6 недель после начала медикаментозной терапии при контрольном ультразвуковом исследовании брюшной полости не было обнаружено роста опухоли, а клинические признаки анорексии исчезли. В клиническом анализе крови во время контрольных исследований периодически отмечалась тромбоцитопения. Других клинико-патологических отклонений не наблюдалось. Спустя 18 месяцев после постановки диагноза у кошки развился сахарный диабет, который хорошо контролировался с помощью инсулина гларгина и диеты с высоким содержанием белка и низким содержанием углеводов. На 792-й день с момента первого обращения владельцы приняли решение об эвтаназии животного из-за прогрессирующей анорексии. Данный клинический случай является первым примером длительного контроля клинических симптомов, таких как анорексия и вялость, а также длительной выживаемости у кошки с карциномой поджелудочной железы при лечении тоцераниба фосфатом1.
Применение тоцераниба и других ингибиторов тирозинкиназы не распространено в лечении кошек11-14. Основные побочные эффекты, наблюдаемые у кошек при использовании тоцераниба, включают миелосупрессию, азотемию, повышение активности аланинаминотрансферазы и нарушение функций желудочно-кишечного тракта11-14. Легкая тромбоцитопения у кошки возникла, вероятно, вследствие искусственного уменьшения количества тромбоцитов, вызванного миелосупрессией, обусловленной применением тоцераниба фосфата. Независимо от причины возникновения тромбоцитопении, у кошки не наблюдалось никаких клинических признаков. Пероральное введение данного препарата позволило снизить частоту визитов к ветеринарному врачу, что способствовало минимизации стресса у животного. Необходимо дальнейшее изучение тоцераниба фосфата и его эффективности в терапии карциномы поджелудочной железы у кошек1.
В ряде зарубежных литературных источников описывается использование комбинации гемцитабина и карбоплатина, однако из-за широкого спектра побочных эффектов, зарегистрированных у пациентов, данный протокол не рекомендуется к применению.
В медицинской литературе упоминается применение препарата «Сунитиниб». Механизм его действия аналогичен тоцераниба фосфату, и он успешно продлевает выживаемость у людей с аденокарциномой поджелудочной железы при использовании в качестве поддерживающей терапии, но не в качестве основного лечения10-14.
Материалы и методы исследований
На первичный прием в ветеринарную клинику поступила 11-летняя кошка (стерилизованная самка, метис), животное не было вакцинировано и не подвергалось обработке от экто- и эндопаразитов. В течение последних шести месяцев у кошки наблюдались симптомы хронической рвоты непереваренным кормом и гипорексии. Владельцы не обращались за ветеринарной помощью и не проводили самостоятельную терапию.При физикальном обследовании кошки было выявлено следующее: дегидратация в пределах 5–6%, шерсть тусклая, признаки себореи, замедленная скорость наполнения капилляров (СНК – 1,5), розовые и умеренно влажные слизистые оболочки, термометрия 38,3 °C, вес 4,8 кг. При пальпации брюшной полости в области эпигастрия было обнаружено объемное образование: неоднородное, плотное, умеренно болезненное.
Диагностика. Для уточнения диагноза и определения тактики лечения были проведены стандартные диагностические исследования: была отобрана кровь из латеральной подкожной вены (v. cephalica) для общего и биохимического анализов, также была выполнена рентгенография грудной клетки (онкопоиск). Общий клинический анализ крови проводился на анализаторе Seamaty Vet Hematology VBC30 с дополнительным ручным подсчетом клеток. Ультразвуковое исследование желудочно-кишечного тракта было выполнено на аппарате Mindray DC-N3 для определения топографии новообразования и исключения метастазов в близлежащие органы.
Результаты исследований и обсуждение
В клиническом анализе крови отмечались тромбоцитопения и повышение палочкоядерных нейтрофилов (абсолютное количество): тромбоциты – 37×109/л (референтный интервал 100–514×109/л), лейкоциты – 12,2×109/л (референтный интервал 5,5–19,5×109/л), палочкоядерные нейтрофилы (абсолютное кол-во) 0,6×109/л (референтный интервал (абсолютное количество) 0–0,3×109/л).В биохимическом анализе крови не отмечалось отклонений, за исключением гипертриглицеридемии – 1,21 ммоль/л (референтный интервал уровня триглицеридов 0–1,13 ммоль/л), повышения уровней общего белка (93,1 г/л) и глобулинов (56,8 г/л) при референтных интервалах 57–89 г/л и 23–52 г/л соответственно.
На рентгенографии грудной клетки, проведенной в трех проекциях (правая латеральная, левая латеральная и одна вентродорсальная), признаков метастазирования не отмечалось.
По результатам ультразвукового исследования желудочно-кишечного тракта, проведенного на аппарате Mindray DC-N3, было выявлено объемное образование в проекции тела поджелудочной железы размером 5,5×5,0 см, неоднородное, смешанной эхогенности.
На основании проведенных обследований был поставлен предварительный диагноз «новообразование поджелудочной железы».
Совместно с владельцами было принято решение о проведении диагностической лапаротомии для забора гистологического материала новообразования и установления патоморфологического диагноза.
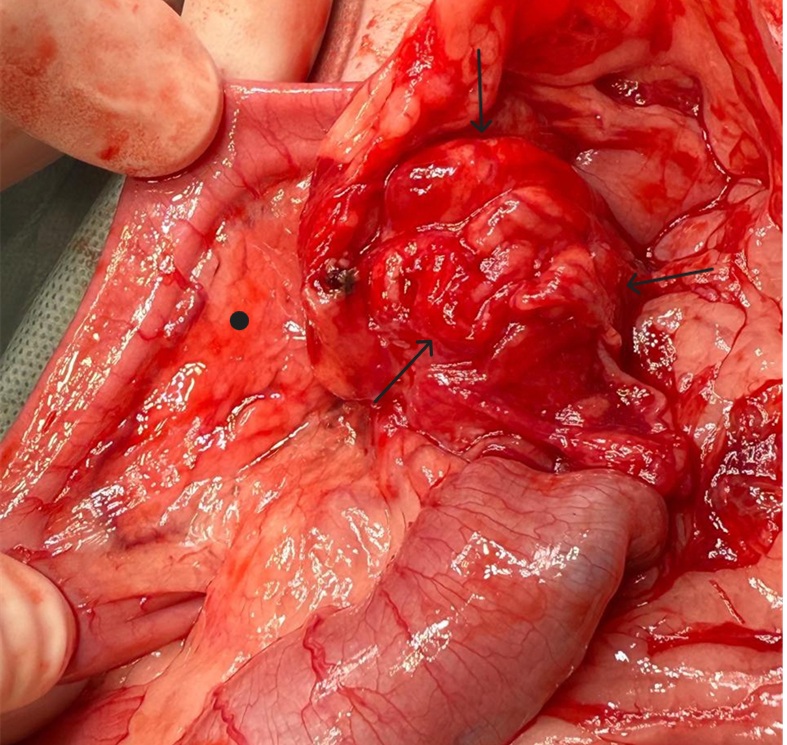
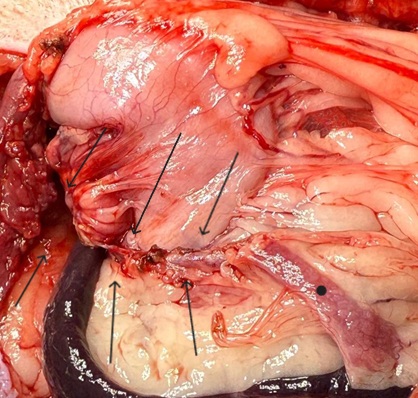
При проведении диагностической лапаротомии (фото 1, 2) было выявлено образование округлой формы в теле поджелудочной железы размером 5,5×5,0 см (начиналось в области пилоруса и переходило к правому краю поджелудочной железы), высокой плотности, бугристое. Тело поджелудочной железы было практически полностью замещено новообразованием, которое также затронуло область сфинктера Одди.
С учетом локализации образования и невозможности его резекции без риска развития полиорганной недостаточности было принято совместное с владельцами решение об эвтаназии пациента интраоперационно.
Результат гистологического исследования эксцизионной биопсии: выявлено высококлеточное инвазивное эпителиальное новообразование с очагами некроза. Структура опухоли характеризуется наличием множества нечетко различимых канальцев, гнезд и тяжей, окруженных неравномерно выраженной фиброваскулярной стромой со смешанной воспалительной инфильтрацией.
Клетки опухоли имеют столбчатую, полигональную или округлую форму со слабой или умеренно развитой эозинофильной цитоплазмой и центральным или апикальным округлым или овальным ядром, содержащим 1–2 хорошо выраженные нуклеолы. Наблюдается умеренный клеточный полиморфизм, а митозы встречаются с частотой 1–3 в поле зрения. Присутствуют очаги плоскоклеточной дифференцировки.
Заключение: низкодифференцированная карцинома поджелудочной железы.
Заключение
Карцинома поджелудочной железы является одним из наиболее агрессивных и трудно поддающихся лечению видов рака у кошек. В современных реалиях золотым стандартом лечения пациентов с карциномами поджелудочной железы является хирургическое вмешательство, включающее широкую резекцию. На основании анализа научных исследований и литературных источников можно сделать вывод о том, что применение химиотерапии и лучевой терапии в большинстве случаев вызывает сомнения и обычно не приносит значительного долгосрочного эффекта.Обеспечение качественной жизни пациентов с опухолями поджелудочной железы представляет собой сложную задачу. Применяемые терапевтические методы часто сопровождаются высокой токсичностью, что может приводить к развитию полиорганной недостаточности. Паллиативные меры, такие как обезболивание, изменение рациона и поддерживающая терапия, направлены на улучшение самочувствия кошки – такой подход особенно важен, когда другие методы лечения невозможны.
Прогноз для кошек с карциномой поджелудочной железы, как правило, неблагоприятный, что обусловлено выраженной инвазивностью и ранним метастазированием, приводящим к срокам выживаемости от нескольких дней до нескольких недель3,4.
Список литературы:
- Andrea Dedeaux. Long-term clinical control of feline pancreatic carcinoma with toceranib phosphate / Andrea Dedeaux, Ingeborg Langohr, Bonnie Boudreaux. The Canadian Veterinary Journal – 2018. Page 751–754.
- Bennett P. F. Ultrasonographic and cytopathological diagnosis of exocrine pancreatic carcinoma in the dog and cat / Bennett P. F., Hahn K. A., Toal R. L., Legendre A. M. Journal Am Anim Hosp Assoc – 2001.
- Brown P. Multifocal necrotizing steatitis associated with pancreatic carcinoma in 3 dogs / Brown P. J., Mason K. V., Merrett D. J., Mirchandani S. and Miller R. I. Journal of Small Animal Practice 35 – 1994. Page 129–132.
- Head K. Histological classification of tumors of the pancreas of domestic animals / Head K., Cullen J., Dubielzig R., et al. Histological Classification of Tumors of the Alimentary System of Domestic Animals – 2003. Page 111–118.
- Jubb K. Pancreas. In: Maxie G., editor. Jubb, Kennedy & Palmer’s Pathology of Domestic Animals. 6th ed / Jubb K., Stent A. – 2016. Page 365–368.
- Seaman R. L. Exocrine pancreatic neoplasia in the cat: A case series. J Am Anim Hosp Assoc. – 2004. Page 238–245.
- Linderman M. J. Feline exocrine pancreatic carcinoma: A retrospective study of 34 cases / Linderman M. J., Brodsky E. M., de Lorimier L. P., Clifford C. A., Post G. S. Vet Comp Oncol. – 2013. Page 208–218.
- Daly M. Safety of masitinib mesylate in healthy cats / Daly M., Sheppard S., Cohen N., et al. J Vet Intern Med. – 2011. Page 297–302.
- Lachowicz J. L. A phase I clinical trial evaluating imatinib mesylate (Gleevec) in tumor-bearing cats / Lachowicz J. L., Post G. S., Brodsky E. J Vet Intern Med. – 2005. Page 860–864.
- Merrick C. H. Retrospective evaluation of toceranib phosphate (Palladia®) toxicity in cats / Merrick C. H., Pierro J., Schleis S. E., et al. Vet Comp Oncol. – 2017. Page 710–717.
- Harper A. Toxicity and response in cats with neoplasia treated with toceranib phosphate / Harper A., Blackwood L. J Feline Med Surg. – 2016. Page 619–623.
- Holtermann N. The tyrosine kinase inhibitor toceranib in feline injection site sarcoma: Efficacy and side effects / Holtermann N., Kiupel M., Hirschberger J. Vet Comp Oncol. – 2016. Page 632–640.
- Olmsted G. A. Tolerability of toceranib phosphate (Palladia) when used in conjunction with other therapies in 35 cats with feline oral squamous cell carcinoma: 2009–2013 / Olmsted G. A., Farrelly J., Post G. S., Smith J. J Feline Med Surg. – 2016. Page 568–575.
- Wiles V. Retrospective evaluation of toceranib phosphate (Palladia) in cats with oral squamous cell carcinoma / Wiles V, Hohenhaus A, Lamb K, Zaidi B, Camps-Palau M, Leibman N. J Feline Med Surg. – 2016. Page 185–193.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург