1. Ветеринарная клиника Ciavdar, г. Кишинев, Молдова.
Вступление
Любые лечебно-диагностические манипуляции в ветеринарной медицине могут сопровождаться осложнениями. Большинство из них хорошо описаны в литературе: известны механизмы развития, факторы риска, способы профилактики и коррекции. Клиницисты, как правило, хорошо ориентируются в частых осложнениях – тех, с которыми они сами сталкивались, которые встречались в практике коллег или регулярно обсуждаются в научных публикациях и на профессиональных мероприятиях. Однако существует другая категория осложнений – редкие осложнения. Их частота настолько низка, что в течение многолетней практики врач может ни разу не столкнуться с ними. Информация о таких событиях редко включается в клинические руководства и обсуждается на профессиональных конференциях, поэтому редкие осложнения часто оказываются вне зоны профессионального внимания1–3. В результате их возникновение может привести к диагностической неопределенности и повышенному уровню тревоги у специалистов. Это особенно характерно для врачей, которые не сталкивались с подобными случаями ни во время обучения, ни на ранних этапах практической деятельности4.Такие ситуации имеют не только клинические, но и психологические последствия. В медицине человека описан феномен «второй жертвы» (англ. second victim) – эмоциональные и когнитивные реакции медицинского работника на непредвиденное неблагоприятное событие. В последние годы этот феномен описывается также и в ветеринарной медицине, в том числе в анестезиологии: неожиданные осложнения усиливают тревогу, снижают уверенность в собственных действиях и иногда провоцируют чрезмерно осторожное, перестраховочное принятие решений, включающее необоснованную диагностическую эскалацию4-6.
Одним из наиболее эффективных способов предотвращения таких реакций считается заблаговременно выстроенная коммуникация с владельцем животного: обсуждение реальных, но низких анестезиологических рисков, методов мониторинга и контроля боли, а также алгоритмов действий в случае осложнений. Подобные рекомендации представлены в руководствах по ветеринарной анестезии и публикациях по управлению неблагоприятными событиями7.
Среди редких, но описанных осложнений регионарных и нейроаксиальных методов анестезии упоминается синдром Хорнера. У собак он зарегистрирован после эпидурального введения местных анестетиков и блокады плечевого сплетения. В большинстве случаев синдром имеет транзиторный характер и его признаки регрессируют в течение нескольких часов, не приводя к долгосрочным последствиям8-10. Однако внезапное появление офтальмологической симптоматики на фоне недавней анестезии может восприниматься как серьезное осложнение, вызывая диагностическую неопределенность и беспокойство как у ветеринарного специалиста, так и у владельца животного.
Представленный клинический случай расширяет имеющуюся доказательную базу, описывая транзиторный синдром Хорнера, возникший после эпидурального введения местного анестетика у собаки. Представлен практический подход к его диагностике, коммуникации с владельцем и предотвращению ненужных диагностических и терапевтических вмешательств при самоограничивающемся характере синдрома.
Клинический случай
Пациент: французский бульдог (самка) в возрасте 1 года и весом 12 кг. Согласно классификации Американского общества анестезиологов (англ. American Society of Anesthesiologists), животное было отнесено к классу риска анестезии I, что соответствует молодому, клинически здоровому пациенту без сопутствующих заболеваний и функциональных нарушений. Хирургическое вмешательство выполнялось как плановая овариогистерэктомия, не связанная с патологическими процессами или жалобами со стороны владельцев. Перед операцией были проведены общий клинический и биохимический анализы крови, а также эхокардиография, которая не выявила отклонений. По данным физикального осмотра собака была клинически стабильна, признаков системных нарушений не отмечалось.Перед началом анестезии был установлен периферический венозный катетер (22 G) и была начата инфузионная терапия кристаллоидным раствором («Стерофундин», 5 мл/кг/ч). Премедикация включала внутривенное введение диазепама в дозе 0,5 мг/кг (6 мг; концентрация 5 мг/мл, объем 1,2 мл). Индукцию проводили с применением пропофола в дозе 6 мг/кг (72 мг; концентрация 10 мг/мл, объем 7,2 мл) до достижения адекватной глубины анестезии и возможности проведения безопасной интубации. Трахея была интубирована эндотрахеальной трубкой диаметром 5,0 мм с манжетой.
Эпидуральная анестезия выполнена на уровне L7–S1. Использовался лидокаин в дозе 4 мг/кг (48 мг; концентрация 20 мг/мл – 2,4 мл), разведенный 0,9%-ным раствором натрия хлорида до конечного объема 0,36 мл/кг (4,3 мл). Препарат вводили однократным болюсом в течение примерно одной минуты, предварительно выполнив аспирационный тест (кровь и ликвор отсутствовали). Поддержание анестезии осуществлялось с помощью севофлурана, подаваемого в кислородно-воздушной смеси. Дыхание пациента оставалось спонтанным. Концентрация севофлурана варьировалась от 2,5% в начале поддержания до 1,5% по мере стабилизации глубины наркоза. Для послойного орошения операционной раны применяли 0,5%-ный раствор бупивакаина.
Интраоперационный мониторинг: электрокардиография (синусовый ритм 80–100 уд/мин), пульсовая оксиметрия (SpO2 в диапазоне 98–100%), концентрация кислорода во вдыхаемой смеси FiO2 (70%), неинвазивное измерение артериального давления (систолическое давление в пределах 99–116 мм рт. ст., среднее давление – 68–85 мм рт. ст.), капнография (EtCO2 в диапазоне 35–40 мм рт. ст.), контроль частоты дыхания (12–15 вдохов в минуту), уровень глюкозы в крови (5,7 ммоль/л). Температура в конце операции составляла 38,0 °C. Для профилактики гипотермии использовались обогреваемый операционный стол и электрические грелки. Длительность анестезии составила 45 минут, хирургического вмешательства – 28 минут.
Овариогистерэктомия была выполнена по стандартной методике, интраоперационных осложнений отмечено не было.
Пробуждение пациента осуществлялось в отделении интенсивной терапии с отсроченной экстубацией, обусловленной породными особенностями. Эндотрахеальная трубка была удалена через 5 минут после поступления пациента в отделение на фоне выраженного кашлевого рефлекса и самостоятельного удержания головы. В послеоперационном периоде осуществлялся мониторинг физиологических параметров: температуры тела, частоты дыхательных движений, частоты сердечных сокращений, артериального давления и уровня болевого синдрома. Для анальгезии был назначен мелоксикам в дозе 0,1 мг/кг подкожно 1 раз в сутки в течение двух дней.
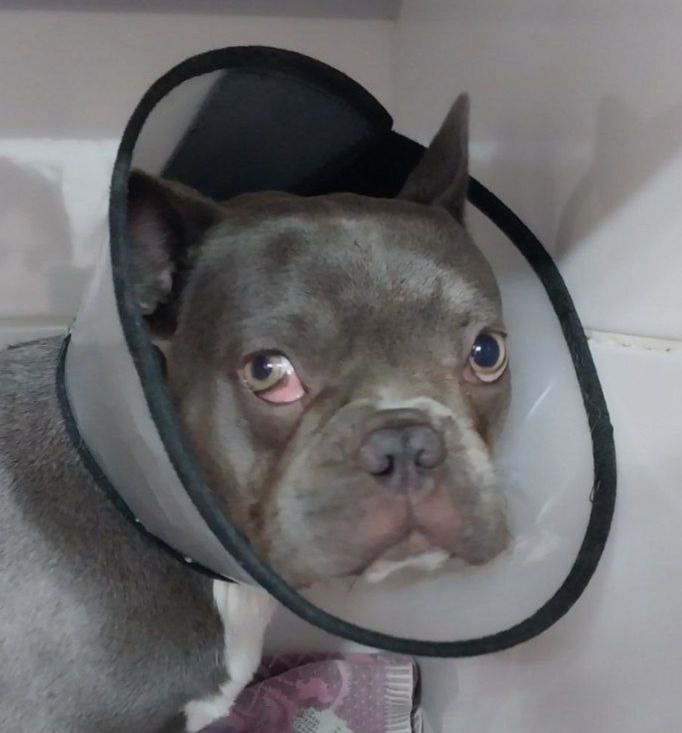
В фазе пробуждения животного отмечались односторонний пролапс третьего века, птоз верхнего века и анизокория: миоз справа, мидриаз слева (рис. 1). Клиническая картина соответствовала правостороннему синдрому Хорнера. Подобное осложнение ранее не наблюдалось в нашей практике, поэтому на этапе первичной оценки связь с эпидуральной анестезией не была очевидной. С учетом внезапного появления изменений при отсутствии неврологических нарушений до операции были рассмотрены дифференциальные диагнозы, способные проявиться остро: фиброзно-хрящевая эмболия или инфаркт ствола головного мозга либо шейного отдела спинного мозга, острый средний или внутренний отит с вовлечением структур барабанной полости, а также идиопатический синдром Хорнера.
После полной экстубации был выполнен неврологический осмотр. Уровень сознания находился в пределах нормы, нарушений функций черепных нервов не было выявлено. Походка и постуральные реакции были сохранены, болевая реакция отсутствовала. При отоскопии наружный слуховой проход был чистым, барабанная перепонка визуализировалась полностью, признаков вестибулярного синдрома не было установлено. Эти данные позволили исключить сосудистые события, фиброзно-хрящевую эмболию и отит.
Несмотря на распространенность идиопатического синдрома Хорнера, в ветеринарной литературе не описано его внезапное развитие непосредственно после анестезии.
С учетом отсутствия других неврологических нарушений был проведен анализ доступных литературных источников, содержащих информацию об аналогичных случаях транзиторного синдрома Хорнера у собак после эпидуральной анестезии. В большинстве описанных ситуаций данное осложнение связывалось с быстрым или чрезмерно объемным введением местного анестетика и его краниальным распространением. В данном случае наиболее вероятным фактором также являлась высокая скорость введения раствора (в течение примерно 1 минуты).
Поскольку выраженные офтальмологические изменения после анестезии могут производить впечатление серьезного осложнения, владельцам животных была предоставлена подробная информация о механизмах возникновения и ожидаемой динамике этих состояний. Было разъяснено, что выявленные признаки соответствуют транзиторному синдрому Хорнера, который не сопровождается болевыми ощущениями и обычно регрессирует в течение нескольких часов, не оставляя долгосрочных последствий. После получения объяснений владельцы приняли рекомендации по домашнему мониторингу состояния животного и покинули клинику, обладая полной информацией о текущем состоянии своего питомца.
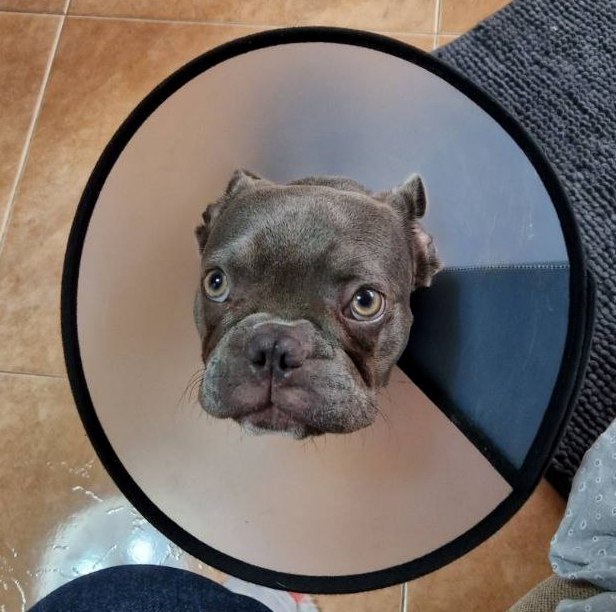
26.06.2025 г. в 18:00 были получены фотографии пациента (рис. 2), на которых отсутствовали признаки анизокории и пролапса третьего века. Состояние животного оценивалось как удовлетворительное, нарушений поведения и зрения не наблюдалось. Быстрое и полное исчезновение симптомов подтвердило первоначальное предположение о транзиторном синдроме Хорнера, связанном с эпидуральной анестезией. Дополнительное вмешательство не потребовалось.
Обзор ветеринарной литературы
Синдром Хорнера/Горнера (англ. Horner’s syndrome) – это феномен, возникающий вследствие дисфункции окулосимпатического пути (симпатической иннервации глаза) и характеризующийся сочетанием миоза, энофтальма, протрузии третьего века и птоза9-12.Нейроанатомия
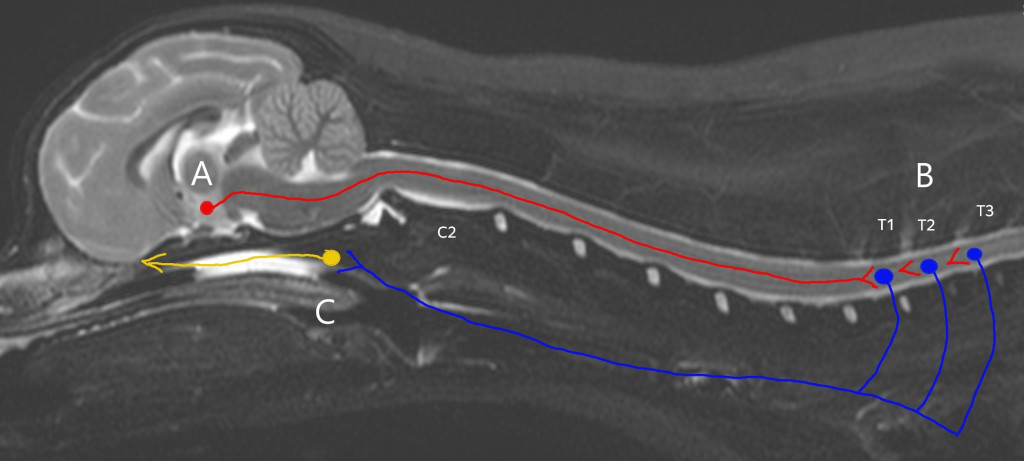
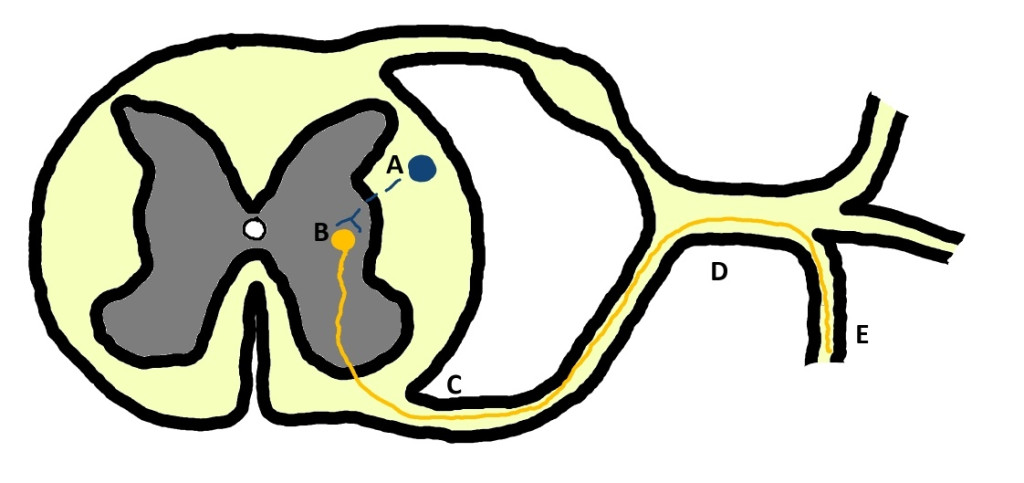
Симпатическая иннервация глаза представляет собой трехнейронную систему. Центральный нейрон, также известный как нейрон первого порядка, располагается в гипоталамусе. Его аксон проходит через ствол мозга и продолжает свой путь в латеральном тектотегментоспинальном (покрышечно-спинальном) тракте, расположенном в латеральном канатике белого вещества спинного мозга12,13,14 (рис. 3). Аксон нейрона первого порядка образует синаптический контакт с преганглионарным нейроном (нейроном второго порядка) в интермедиалатеральном роге серого вещества первых трех грудных сегментов спинного мозга12. Аксон преганглионарного нейрона (нейрона второго порядка) покидает спинной мозг в составе вентральных нервных корешков (Т1, Т2, Т3; рис. 4) и проходит небольшое расстояние в составе спинномозгового нерва, после чего отделяется в виде соединительной ветви (лат. ramus communicans) в месте, где спинномозговой нерв латерально от межпозвоночного отверстия делится на дорсальную и вентральную ветви12,15. Далее соединительная ветвь входит в грудной отдел симпатического ствола, располагающегося вентролатерально по отношению к телам позвонков. Симпатический ствол продолжается краниально в пределах дорсального средостения, проходя через шейно-грудной ганглий, локализованный в области поверхности краниальной доли легкого, и далее к среднему шейному ганглию12,15. При прохождении через оба этих ганглия синаптическая передача не осуществляется (не образует синапсов). На уровне краниальной апертуры грудной клетки (вход в грудную клетку) симпатический ствол объединяется с блуждающим нервом в пределах общего эпиневрия12. Затем вагосимпатический ствол направляется краниально к голове, проходя по латеральной поверхности трахеи, после чего симпатический ствол отделяется от блуждающего нерва и заканчивается в краниальном шейном ганглии12,14. Краниальный шейный ганглий располагается вентромедиально по отношению к барабанной булле, здесь аксон преганглионарного нейрона образует синаптический контакт с телом постганглионарного (третьего порядка) нейрона12. Синаптическая передача в ганглии осуществляется с участием ацетилхолина, который высвобождается преганглионарными телодендриями и связывается с никотиновыми холинергическими рецепторами на теле постганглионарного нейрона12,15.Путь аксонов постганглионарного нейрона описан не столь четко, как путь проксимальных отделов окулосимпатического пути. После выхода аксонов из краниального шейного ганглия они образуют сплетение вокруг внутренней сонной артерии12,15. Часть волокон проходит через барабанную буллу по вентральной поверхности каменистой части височной кости, в то время как другие идут медиальнее буллы, прежде чем войти в полость черепа12,14. Постганглионарные волокна могут также сопровождать внутреннюю сонную артерию и проникать в полость черепа через тимпаноокципитальную щель и сонный канал12,14,16.
Достигнув полости черепа, постганглионарные волокна проходят вентрально от тройничного ганглия и покидают череп вместе с глазничной ветвью тройничного нерва через глазничную щель, направляясь в орбиту12,14,16,17. Далее эти волокна образуют носоресничный нерв, а в итоге – длинный ресничный нерв, который иннервирует мышцу, расширяющую зрачок и кровеносные сосуды увеального тракта12. Кроме того, волокна обеспечивают симпатическую иннервацию гладких мышц периорбиты и век. У кошек существует симпатическая иннервация гладких мышц третьего века, отсутствующая у собак12,15.
Часть постганглионарных волокон отходит от краниального шейного ганглия в составе наружной сонной артерии и иннервирует артерии головы и ушей, а также потовые железы12. На уровне синапсов между постганглионарными телодендриями и эффекторными органами медиатором выступает норадреналин, взаимодействующий с α-адренергическими рецепторами12,15.
A – гипоталамус и нейрон первого порядка; аксон проходит через ствол мозга и далее в латеральном тектотегментоспинальном тракте.
B – первые три грудных сегмента спинного мозга и нейрон второго порядка; преганглионарный аксон покидает спинной мозг, направляется краниально, объединяется с блуждающим нервом и образует вагосимпатический ствол.
C – область среднего уха и нейрон третьего порядка; постганглионарные волокна иннервируют структуры глаза.
Клинические признаки синдрома Хорнера
Синдром Хорнера классифицируют в зависимости от уровня поражения окулосимпатического пути и локализации – центральный, преганглионарный или постганглионарный. Однако у мелких домашних животных клинические признаки синдрома Хорнера будут идентичными независимо от локализации поражения. Следует отметить, что при центральном поражении маловероятно, что синдром Хорнера будет единственным клиническим симптомом. Другие ожидаемые неврологические нарушения при поражении ствола мозга или спинного мозга включают изменение ментального статуса, парез, нарушение постуральных (позотонических) реакций или дисфункцию других черепных нервов. Центральное поражение также может сопровождаться атаксией. Характер атаксии, скорее всего, будет проприоцептивным, что обусловлено одновременным вовлечением общих проприоцептивных путей, проходящих через спинной мозг и ствол мозга. Часть этих путей располагается в латеральном канатике и находится в непосредственной близости к тектотегментоспинальному тракту12,14. При значительном распространении патологического процесса может быть затронута центральная вестибулярная система, что приводит к более выраженной вестибулярной атаксии12,14.Миоз пораженного глаза является наиболее часто выявляемым признаком синдрома Хорнера и развивается вследствие утраты иннервации мышцы, расширяющей зрачок12. Сфинктер зрачка, иннервируемый парасимпатическим компонентом III пары черепных нервов, при этом функционирует без противодействия и вызывает сужение зрачка12. Мышца, расширяющая зрачок, обладает уникальной особенностью – она получает двойную иннервацию как со стороны симпатической, так и со стороны парасимпатической нервной системы12,15. Симпатическая иннервация обеспечивает сокращение мышцы и расширение зрачка, тогда как парасимпатическая иннервация, напротив, тормозит ее сокращение. При нарушении симпатического пути ингибирующий эффект парасимпатической системы дополнительно препятствует расширению зрачка и усиливает миоз12,15.
При одностороннем поражении развивается анизокория, наиболее заметная в условиях низкой освещенности, поскольку пораженный глаз не способен расширить зрачок в той же степени, что и нормальный12,17. Однако сохранный сфинктер зрачка позволяет пораженному глазу адекватно сужать зрачок при ярком освещении: в хорошо освещенном помещении анизокория может быть практически незаметной. Зрачковые реакции на свет и зрительные функции при этом сохраняются12.
Птоз (то есть опущение верхнего века) приводит к сужению глазной щели на пораженном глазу12. Традиционно считается, что птоз развивается из-за утраты симпатического тонуса в тонких мышечных волокнах век (иногда обозначаемых как мышца Мюллера)12,18. Однако, по мнению некоторых авторов, у собак и кошек эта мышца не играет значительной роли, и птоз является вторичным по отношению к энофтальму12.
Энофтальм. Кольцевые периорбитальные гладкие мышцы помогают поддерживать глазное яблоко в переднем положении внутри орбиты12,14,15. При утрате симпатической иннервации этих мышц происходит их расслабление. В результате мышца, втягивающая глазное яблоко (лат. retractor bulbi), лишается антагонистического влияния и активно втягивает глаз внутрь орбиты, вызывая энофтальм12.
Протрузия третьего века. Хотя степень пролапса третьего века варьируется в разных случаях, это второй по частоте описанный клинический признак синдрома Хорнера12. У собак пролапс носит пассивный характер и является следствием энофтальма12. У кошек имеется дополнительный активный компонент, обусловленный наличием симпатически иннервируемой гладкой мышцы внутри третьего века. При нарушении симпатической иннервации эта мышца больше не способна удерживать третье веко в нормальном (втянутом) положении12,15,17.
Синдром Хорнера как последствие эпидуральной анестезии
Частота развития синдрома Хорнера при применении эпидуральной анестезии значительно варьируется в зависимости от вида и клинической группы. В человеческой популяции зарегистрированная встречаемость синдрома Хорнера составляет приблизительно 1 случай на 10 000 эпидуральных процедур, при этом подавляющее большинство описанных случаев связано с акушерскими протоколами обезболивания родов и кесарева сечения19. У рожениц синдром Хорнера фиксируется заметно чаще: в отдельных сериях – 0,4% при вагинальных родах и до 4% при кесаревом сечении под эпидуральной анестезией20. В ветеринарной анестезиологии статистика синдрома представлена в основном единичными клиническими описаниями: у собак эпидурально-индуцированный синдром Хорнера считается редким явлением и регистрируется в виде отдельных случаев при люмбосакральной или торакальной эпидуральной анальгезии9,22.Предполагаемым механизмом развития синдрома Хорнера после эпидуральной анестезии считается краниальное распространение местного анестетика по эпидуральному пространству до уровня C8-T1, где проходят преганглионарные симпатические волокна, иннервирующие структуры глаза и орбиты19,20. В акушерстве этому способствуют анатомо-физиологические изменения во время беременности: дилатация эпидуральных вен и уменьшение объема эпидурального пространства, возникающие из-за частичной компрессии нижней полой вены, что способствует более легкому распространению раствора вверх20.
К дополнительным факторам, повышающим риск высокого блока, причисляют больший объем и болюсное введение препарата, положение пациента в латеральной декубитальной позиции (латерализация синдрома отмечалась на той стороне, на которой лежал пациент), а также использование катетерных техник с повторным дозированием. Эти факторы неоднократно приводили к развитию транзиторного одностороннего или двустороннего синдрома Хорнера и у людей, и у собак19,21,22. В ветеринарных источниках предполагается аналогичный механизм распространения раствора к шейно-грудному отделу спинного мозга9,22.
В подавляющем большинстве описанных случаев синдром Хорнера после эпидуральной анестезии имеет кратковременный и полностью обратимый характер, не требующий специфического лечения. У людей симптомы обычно появляются в течение первых минут или часов после введения болюса или усиления инфузии и спонтанно исчезают в среднем в пределах 2–4 часов, хотя в литературе отмечены колебания от нескольких минут до 24 часов19. В обзоре акушерских наблюдений подчеркивается, что состояние считается «относительно доброкачественным», а основная тактика при его возникновении – наблюдение и исключение других причин, поскольку синдром регрессирует без последствий после уменьшения концентрации анестетика или остановки инфузии20. Аналогично у пациентов с торакальной эпидуральной анальгезией, применяемой при абдоминальных операциях, прекращение или снижение скорости введения препарата приводит к полной регрессии симптомов в течение нескольких часов21,22.
У животных описаны единичные транзиторные случаи: у собак синдром Хорнера полностью исчезал после прекращения действия препарата без необходимости медикаментозного вмешательства и без остаточных неврологических явлений, что рассматривается как доброкачественное и самоограничивающееся осложнение9.
Таким образом, при стабильно нормальных показателях гемодинамики и отсутствии других неврологических симптомов лечение не требуется, а ведение пациента ограничивается наблюдением.
Выводы
Несмотря на то что синдром Хорнера после эпидуральной анестезии остается редким осложнением как у людей, так и у животных, выраженные косметические проявления (миоз, птоз, энофтальм и пролапс третьего века) могут выглядеть драматично и вызывать тревогу у врача и владельца. Тем не менее, согласно литературным данным, подчеркивается его доброкачественный и транзиторный характер с самопроизвольным восстановлением в пределах нескольких часов, обычно не превышая 24 часов19,20. Если у пациента отсутствуют другие симптомы поражения центральной или периферической нервной системы, такие как проприоцептивная или вестибулярная атаксия, нистагм, наклон головы, судороги, стойкие нарушения движений грудных конечностей, а также если выраженность синдрома Хорнера уменьшается в типичные сроки, дополнительная диагностика не требуется и ведение пациента ограничивается наблюдением21,22. Напротив, отсутствие положительной динамики или появление других неврологических симптомов служит основанием для расширенного обследования с целью исключения альтернативных причин.Список литературы:
- Griffon D., Hamaide A. (ed.). Complications in small animal surgery. John Wiley & Sons, 2016.
- Follette C. M. et al. A systematic review of criteria used to report complications in soft tissue and oncologic surgical clinical research studies in dogs and cats //Veterinary Surgery. – 2020. – Т. 49. – № 1. – С. 61–69.
- Portier K., Ida K. K. Anesthetic risk and complications in veterinary medicine //Frontiers in Veterinary Science. – 2020. – Т. 7. – С. 397.
- Kittisiam T. et al. A qualitative exploration of the emotional experiences and applications of emotional intelligence in early‐career veterinarians //Veterinary Record. – 2025. – С. e5599.
- Santos L. C. P. et al. Psychological, physical, and professional impact on second victims in veterinary anaesthesia: a cross-sectional international survey-Part 1 //Veterinary Anaesthesia and Analgesia, 2024.
- Lane M. A. et al. Supporting clinicians after adverse events: development of a clinician peer support program //Journal of patient safety. – 2018. – Т. 14. – № 3. – С. e56-e60.
- Grubb T. et al. 2020 AAHA anesthesia and monitoring guidelines for dogs and cats //Journal of the American Animal Hospital Association. – 2020. – Т. 56. – № 2. – С. 59–82.
- Bianchi C., Stathopoulou T. R. Transient unilateral Horner’s syndrome after epidural catheter administration of bupivacaine in a dog //Veterinary Anaesthesia and Analgesia. – 2021. – Т. 48. – № 4. – С. 628–629.
- Bosmans T. et al. Transient unilateral Horner’s syndrome after epidural ropivacaine in a dog //Veterinary Anaesthesia and Analgesia. – 2009. – Т. 36. – № 4. – С. 401–406.
- Chohan A. S. Anesthesia case of the month //Journal of the American Veterinary Medical Association. – 2019. – Т. 255. – № 9. – С. 1016–1018.
- Won-gyun S. Evaluation of Factors Influencing Epidural Anesthesia in Dogs, 2015.
- Zwueste D. M., Grahn B. H. A review of Horner’s syndrome in small animals //The Canadian Veterinary Journal. – 2019. – Т. 60. – № 1. – С. 81.
- Viscasillas J. et al. Transient Horner′ s syndrome after paravertebral brachial plexus blockade in a dog //Veterinary anaesthesia and analgesia. – 2013. – Т. 40. – № 1. – С. 104–106.
- De Lahunta A., Glass E. N., Kent M. de Lahunta's Veterinary Neuroanatomy and Clinical Neurology-E-Book. – Elsevier Health Sciences, 2020.
- Evans H. E., De Lahunta A. Miller's anatomy of the Dog-E-Book: Miller's anatomy of the Dog-E-Book. – Elsevier health sciences, 2012.
- Jones S. M. P. Neuro-ophthalmology, 1989.
- Penderis J. Diagnosis of Horner's syndrome in dogs and cats //In Practice. – 2015. – Т. 37. – № 3. – С. 107–119.
- Walton K. A., Buono L. M. Horner syndrome //Current opinion in ophthalmology. – 2003. – Т. 14. – № 6. – С. 357–363.
- Biousse V., Guevara R. A., Newman N. J. Transient Horner's syndrome after lumbar epidural anesthesia //Neurology. – 1998. – Т. 51. – № 5. – С. 1473–1475.
- Vogiatzaki T. et al. Horner’s syndrome and epidural anesthesia in labor and cesarean section //Clin Exp Obstet Gynecol. – 2017. – Т. 44. – № 3. – С. 337–340.
- Holck G., Quaye A. N. Alternating bilateral Horner’s syndrome during continuous thoracic epidural analgesia //Anaesthesia reports. – 2022. – Т. 10. – № 1. – С. e12147.
- Atoot A. et al. Horner's syndrome secondary to epidural anesthesia after scoliosis correction: a case report //Cureus. – 2021. – Т. 13. – № 12.


 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург