Введение
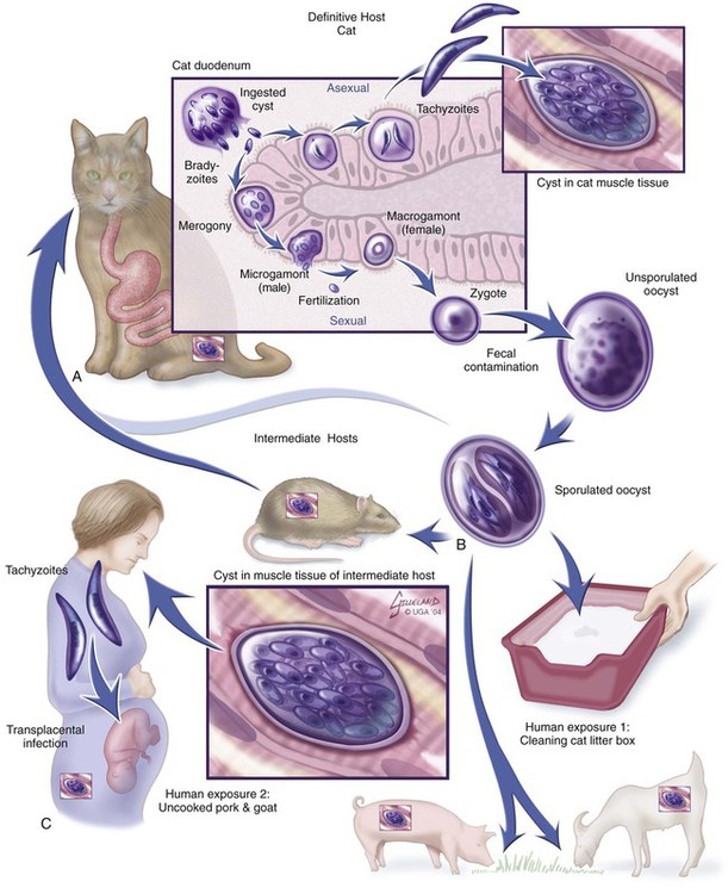
Toxoplasma gondii – облигатный внутриклеточный паразит, вызывающий токсоплазмоз у теплокровных животных и человека. Кошки являются единственными окончательными хозяевами данного паразита, в организме которых происходит его половое размножение. Однако кошки также могут выступать в роли промежуточных хозяев наряду с другими теплокровными видами животных11.Жизненный цикл токсоплазм (рис. 1):
- Окончательный хозяин (кошки и другие представители семейства кошачьих)
Кошка выделяет ооцисты в течение 1–3 недель после заражения. Ооцисты становятся заразными через 1–5 дней после выделения (споруляция) при условии их нахождения в теплой влажной среде. Спорулированные ооцисты обладают высокой устойчивостью к условиям окружающей среды и сохраняют жизнеспособность как в воде, так и в сухих условиях в течение нескольких месяцев18.
- Окружающая среда и промежуточные хозяева
Формирование цист происходит следующим образом: ооцисты или брадизоиты, содержащиеся в проглоченных тканевых цистах, проникают в эпителий кишечника хозяина и трансформируются в тахизоиты, которые активно делятся и распространяются по различным органам и тканям организма. По мере развития иммунного ответа хозяина токсоплазмы замедляют деление и образуют тканевые цисты, содержащие брадизоиты. Эти цисты могут сохраняться в мышцах, мозге и других тканях на протяжении длительного периода времени, а иногда в течение всей жизни хозяина19.
Также возможно вертикальное заражение – при передаче инфекции трансплацентарно11.
У большинства животных инфекция протекает субклинически12. Однако при иммунодефицитных состояниях, таких как коинфекция вирусом иммунодефицита кошек (ВИК), вирусом лейкемии кошек (ВЛК), хронические заболевания, длительная терапия глюкокортикостероидами или другими иммуносупрессорами (в том числе химиотерапевтическими препаратами) и трансплантация почек, возможно развитие клинически значимого системного токсоплазмоза с поражением различных органов, включая ЦНС14,13.
В литературе описано несколько случаев клинического токсоплазмоза у кошек в сочетании с ВИК16 и ВЛК17. В научных экспериментах (Davidson M. G. et al., 1993) изучалось потенциальное влияние вируса иммунодефицита кошек на развитие острого генерализованного токсоплазмоза20. Авторы выяснили, что у кошек с бессимптомным ВИК, искусственно инфицированных тахизоитами Toxoplasma gondii развивается выраженное нарушение клеточно-опосредованного иммунитета (снижение количества CD4+, CD8+ и B-клеток), которое делает их неспособными контролировать репликацию Toxoplasma gondii и предрасполагает к тяжелому, генерализованному токсоплазмозу. При этом у кошек, зараженных только T. gondii (без ВИК), или у кошек, зараженных только ВИК, такого иммунологического эффекта не наблюдалось. Снижение количества и нарушение функции CD4+ T-лимфоцитов ослабляет клеточный иммунный ответ и резко уменьшает продукцию интерферона-гамма (IFN-γ) – ключевого цитокина, необходимого для активации макрофагов и подавления размножения тахизоитов. CD8+ T-клетки в норме ограничивают острую репликацию паразита и поддерживают контроль над латентными тканевыми цистами, что становится невозможным в условиях низкого количества и дисфункции данных клеток. В результате при первичном заражении T. gondii или реактивации латентной инфекции у ВИК-позитивных кошек нарушается способность ограничивать репликацию паразита, что приводит к бесконтрольному размножению тахизоитов и системному поражению органов20.
В одном исследовании (Pena H. F. J. et al., 2017), посвященном описанию клинического случая фатального токсоплазмоза у иммунокомпрометированной кошки, описывалось потенциальное влияние вируса лейкоза кошек на клетки иммунной системы. Авторы упомянули, что данный вирус способен вызывать атрофию тимуса и костного мозга, что приводит к лимфопении, нейтропении и истощению популяции CD4+ и CD8+ лимфоцитов (Ogilvie S. et al., 1988; Lutz W. et al., 2009)17. Схожие иммунологические изменения были описаны в другом исследовании (Davidson M. et al., 1993)20.
Распространенными проявлениями токсоплазмоза у кошек являются спленомегалия, лимфаденопатия, интерстициальная пневмония, менингоэнцефалит, гепатит, холангиогепатит, поражения глаз, миокардит.
Церебральная форма токсоплазмоза у кошек встречается редко (а у собак практически не описана), но характеризуется тяжелым течением, высоким уровнем рецидивов и летальности. Поражения нервной системы могут проявляться как многоочаговым энцефалитом/миелитом, так и образованием локализованных гранулем, имитирующих опухолевые процессы.
Клинический случай
Общие сведения
В июле 2025 года в ветеринарную клинику Сложного случая поступил 7,5-летний кот (метис) с жалобами со стороны владельцев на выраженную вялость, дезориентацию, шаткость походки, снижение аппетита. Короткие самоограничивающиеся эпизоды (5–7 дней) снижения активности и аппетита владельцы отмечали и ранее – в январе, мае, июне. В анамнезе пациента отмечены хронический холангиогепатит, нефролитиаз, хронический нефрит, хронический бронхит. Также за 2,5 года до обращения в клинику у кота был диагностирован вирусный иммунодефицит кошек (ВИК) – уровень антител IgG к ВИК составлял 36,5 при отрицательном результате до 9. В связи с этим пациент получал долутегравир («Тивикай») в дозировке 2,5 мг/кг 1 раз в сутки. В то же время у кота был выявлен высокий уровень антител IgM к возбудителю токсоплазмоза (14,2 при отрицательном результате до 9), и в течение 2 месяцев кот получал клиндамицин в дозе 12,5 мг/кг 2 раза в сутки, несмотря на отсутствие явных клинических признаков токсоплазмоза. По завершении курса лечения клиндамицином уровень антител IgM к возбудителю токсоплазмоза составлял 12,7 (при отрицательном результате до 9), а уровень IgG – 3,6 (при отрицательном результате до 0,9). В связи с отсутствием жалоб дальнейшее лечение токсоплазмоза не проводилось.Результаты неврологического осмотра (июль 2025 года): уровень сознания – оглушение; ментальный статус – дезориентация, навязчивое хождение; отсутствует реакция на угрожающий жест билатерально; слабовыраженный позиционный ротационный нистагм; проприоцепция сохранена. Температура тела – 38,0 °C, ЧСС – 194 уд/мин, АД – 154/95 мм рт. ст., УГК – 10,8 ммоль/л.
По результатам неврологического осмотра был поставлен топический диагноз «поражение переднего мозга слева и продолговатого мозга/мозжечка». Также были проведены рутинные обследования: клинический и биохимический анализы крови, обзорное ультразвуковое исследование (УЗИ) брюшной полости, тонометрия. Результаты этих обследований не выявили клинически значимых отклонений. С учетом отсутствия явных экстракраниальных причин, способствующих развитию данного состояния, пациенту была назначена магнитно-резонансная томография (МРТ) головного мозга с контрастом.
Диагностика
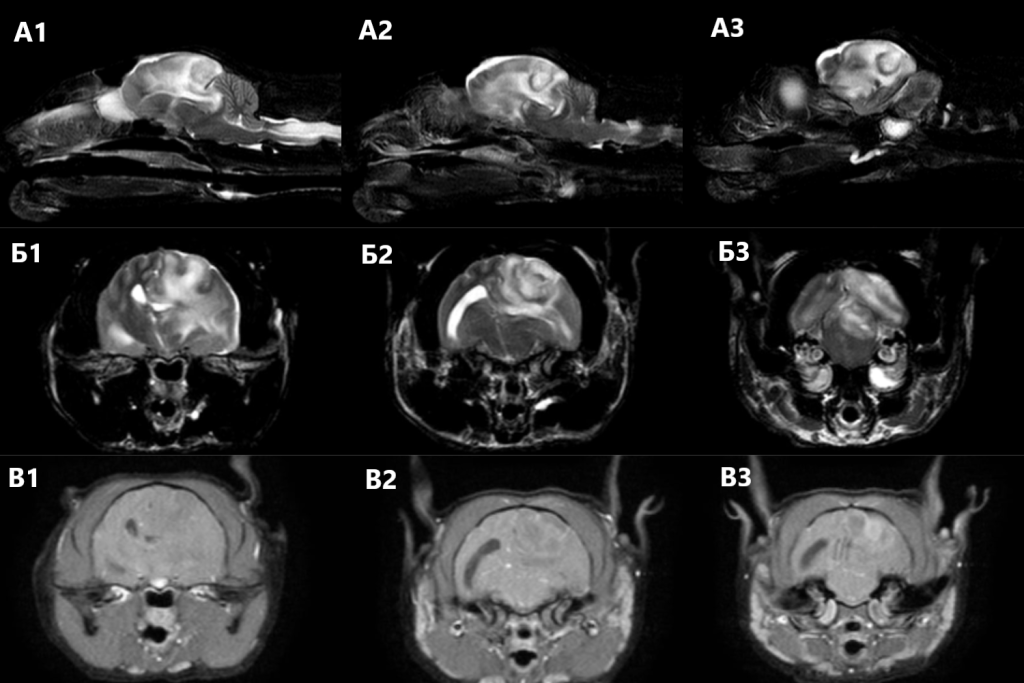
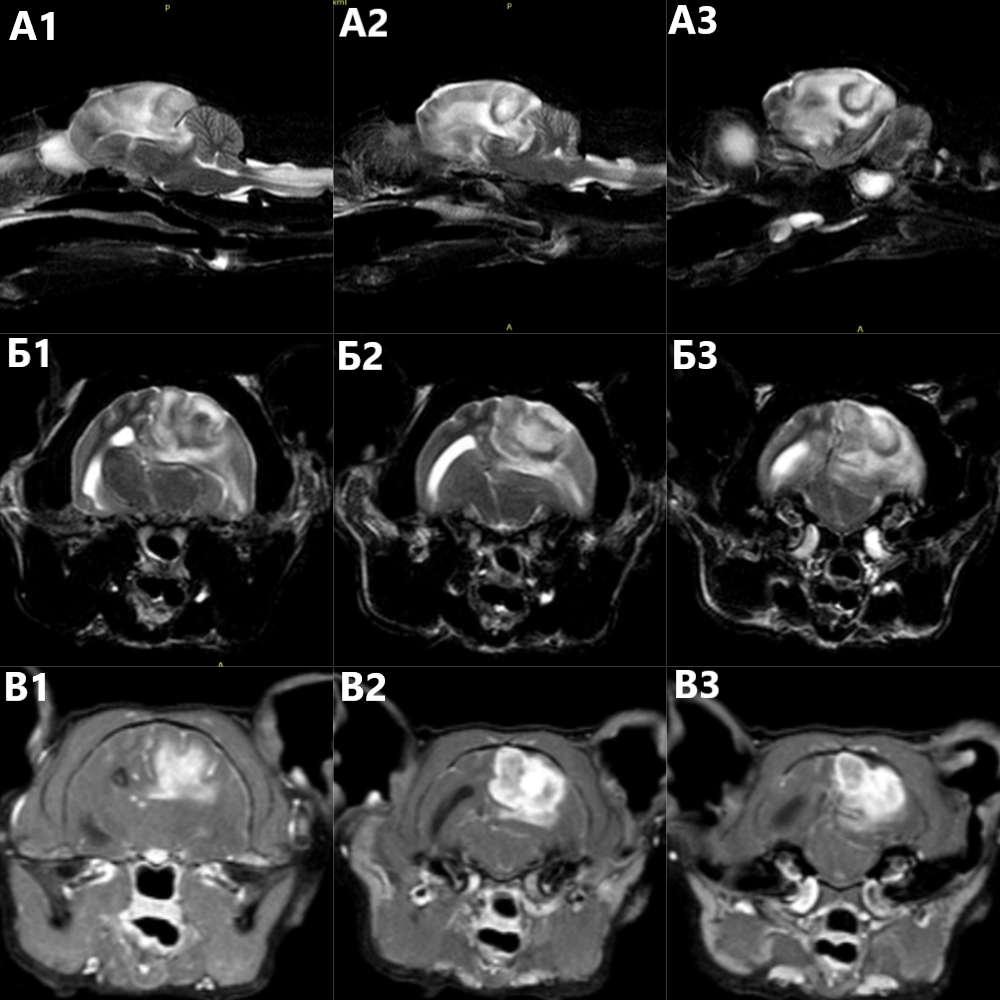
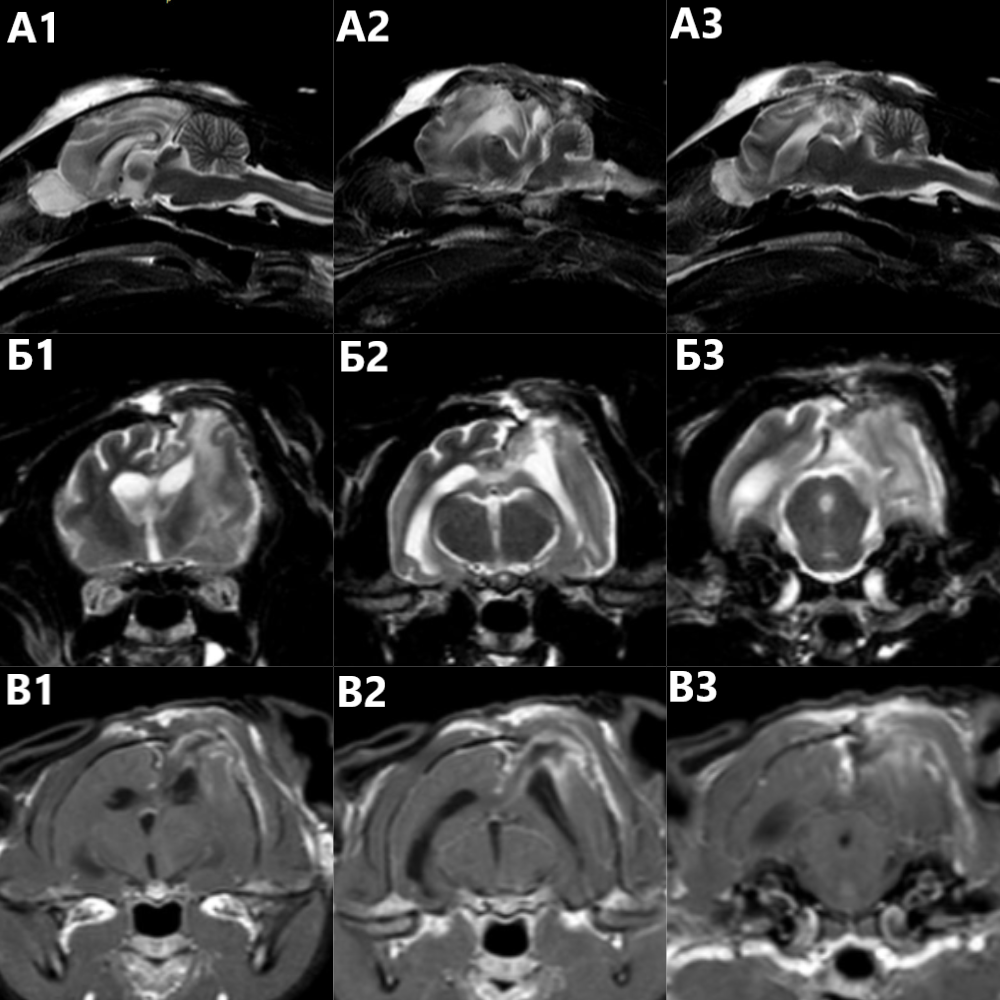
МРТ головного мозга с контрастным усилением выявила объемное интрааксиальное образование в области левой теменной и затылочной долей с выраженным перифокальным отеком, распространяющимся на все левое полушарие, масс-эффектом, смещением срединных структур слева направо, транстенториальным вклинением, вклинением червя мозжечка в большое затылочное отверстие. Накопление контраста образованием слабое, границы образования местами не определяются. На Т2-взвешенных изображениях в трансверсальной плоскости отмечается расширение субарахноидального пространства по периметру левого полушария. Также выявлены сирингомиелия в шейном отделе спинного мозга и двусторонний средний отит (рис. 2).На основании результатов МРТ предполагались следующие дифференциальные диагнозы: глиальное новообразование головного мозга, менингоэнцефалит (менее вероятный диагноз). Первичная тактика лечения была направлена на снижение внутричерепного давления и уменьшение перифокального отека с последующим динамическим контролем посредством проведения повторной МРТ. Для этого применялись маннитол в дозе 1,5 г/кг внутривенно каждые 8 часов в течение суток и преднизолон в дозе 1 мг/кг в сутки. На фоне терапии отмечалось временное улучшение состояния, однако спустя шесть дней состояние вновь ухудшилось. В связи с этим повторно была выполнена МРТ головного мозга с контрастным усилением. Данное исследование выявило увеличение линейных размеров образования и усиление интенсивности накопления контрастного препарата. Остальные нарушения – без динамики (рис. 3). На основании ухудшения неврологического статуса пациента и отрицательной динамики по данным МРТ было принято решение о проведении хирургического удаления образования. Предварительно была выполнена КТ-ангиография с целью онкологического скрининга. По результатам КТ неопластических поражений внутренних органов выявлено не было.
Хирургическое лечение
Выполнена широкая левосторонняя ростротенториальная краниотомия. Поскольку при визуальной оценке кора головного мозга в зоне предполагаемого доступа оставалась внешне интактной и новообразование не визуализировалось напрямую, была предпринята попытка интраоперационной ультразвуковой навигации. Однако использование УЗ-системы не дало дополнительной диагностической информации: образование оказалось изоэхогенным, его эхогенность не отличалась от эхогенности окружающей паренхимы головного мозга, поэтому определить очаг и его границы ультразвуковым методом не удалось. На основании данных предоперационной МРТ было спланировано и выполнено кортикальное окно в проекции очага. На глубине ≈ 3 мм выявлена плотная серовато-белая ткань с выраженной адгезией к окружающей паренхиме. Было выполнено максимально полное макроскопическое удаление патологически измененной ткани. Операционный материал был направлен на патоморфологическое исследование, включающее цитологический и гистологический анализы.Результаты исследований патологического материала
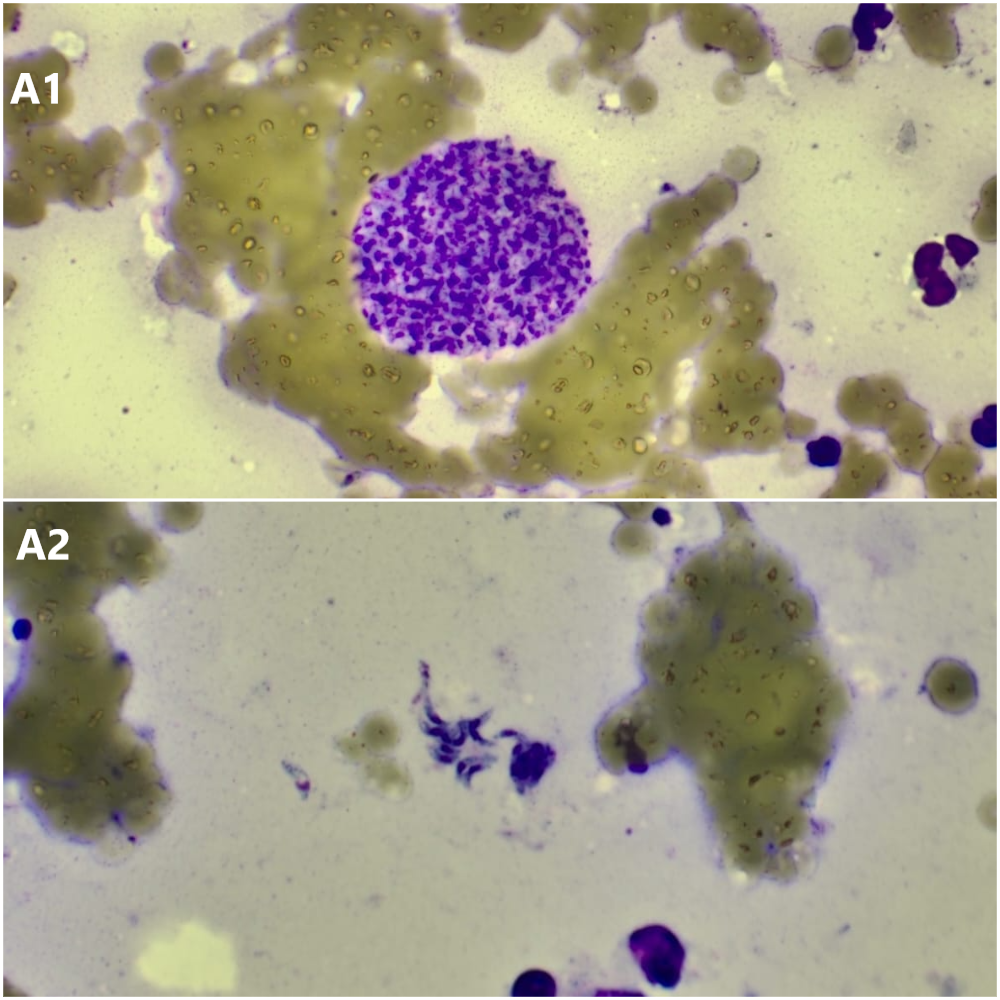
Цитологическая картина: на фоне выраженного количества эритроцитов присутствуют разрозненно лежащие единичные веретеновидные клетки, также выявляются активированные макрофаги с цитофагией и фагоцитозом мелких объектов в форме полумесяца с мелкой округлой структурой внутри (морфологически схожие с брадизоитами токсоплазмы), такие же объекты лежат свободно между клетками. Кроме того, в препарате присутствуют крупные шаровидные зернистые структуры с мелкими фиолетовыми включениями внутри (киста с брадизоитами; рис. 4).Заключение: смешанное воспаление, ассоциированное с паразитарной инвазией Toxoplasma gondii.
На основании результатов цитологического исследования было принято решение о проведении анализа материала со стекол методом ПЦР для диагностики токсоплазмоза. Результат ПЦР оказался положительным.
Одновременно с получением результатов цитологического исследования у пациента была взята кровь для определения уровня антител (IgG + IgM) к возбудителю токсоплазмоза. Результат: уровень IgM составил 6,9, что при коэффициенте К < 9 указывает на отсутствие инфекции; уровень IgG – 2,8, что при коэффициенте К > 1,1 свидетельствует либо о начальном периоде первичной инфекции, либо об инфекции, перенесенной ранее.
Гистологическое исследование также выявило некротический и макрофагальный энцефалит с накоплением структур, морфологически сходных с Toxoplasma.
Послеоперационный период
При поступлении в ОРИТ уровень сознания пациента – кома, спонтанное дыхание не регистрировалось, пациент находился на аппарате ИВЛ. Наблюдались нерегулярные подергивания ушами и движения языком, глотательный рефлекс отсутствовал. Через 12 часов после хирургического вмешательства отмечалась положительная динамика относительно глотательного рефлекса, наблюдались нерегулярные попытки спонтанного дыхания. Спустя сутки после операции уровень сознания улучшился до ступора, дыхание стало продуктивным, пациент был отлучен от аппарата ИВЛ, появились слабопродуктивные попытки самостоятельного изменения положения тела. Через 1,5 суток после операции уровень сознания улучшился до оглушения, пациент начал предпринимать попытки самостоятельного перемещения по клетке.На третьи сутки после операции была проведена повторная МРТ для оценки степени удаления образования. По результатам МРТ в височно-теменной области слева определялись следы оперативного доступа, в костный дефект частично выпадали участки левой теменной и височной долей, левый латеральный желудочек был деформирован. Наблюдался отек белого вещества левого полушария. Положительная динамика отмечалась в отношении транстенториального смещения, смещения червя мозжечка в большое затылочное отверстие и сирингомиелии.
На основании данных МРТ степень удаления образования была оценена как полная или почти полная (рис. 5).
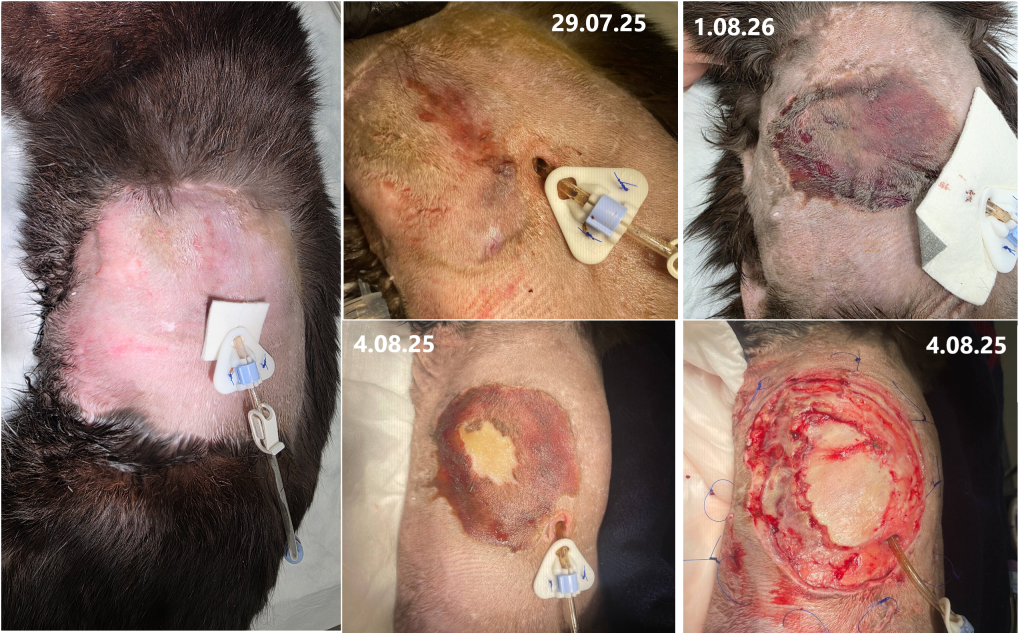
В раннем послеоперационном периоде у пациента развилось обширное поражение мягких тканей (некроз) в области левой латеральной поверхности грудной клетки (рис. 6). Через 12 дней после хирургического вмешательства пациент скончался. Смерть была расценена как не связанная с первичным внутричерепным заболеванием и, вероятнее всего, была обусловлена осложнениями, возникшими вследствие длительной госпитализации и проведения энтерального кормления. У животного развился выраженный некроз мягких тканей в области гастростомы, после этого наблюдалось клиническое ухудшение, лучше всего объясняемое сепсисом, который и был признан наиболее вероятной причиной смерти.
Обсуждение
Церебральный токсоплазмоз у кошек – редкая форма заболевания, описанная в ограниченном числе научных публикаций. Анализ литературы показал, что поражения нервной системы, вызванные простейшими T. gondii, в принципе встречаются довольно редко.В одном из отчетов описана 6-летняя бирманская кошка с полинейропатией, подтвержденной электронейромиографией (ЭНМГ). Кошка не имела доступа к улице, ее рацион состоял из коммерческого корма. Результаты исследований на ВИК и ВЛК были отрицательными, однако у кошки были выявлены высокие титры антител IgG и IgM к T. gondii, измеренные методом непрямой иммунофлюоресценции (1:200 и 1:160 соответственно). Лечение клиндамицином в дозе 18,3 мг/кг 2 раза в сутки привело к положительному клиническому ответу. Через год у кошки случился рецидив симптомов при отрицательных титрах антител, но с положительным ответом на клиндамицин5.
В 2023 году была опубликована статья (Florian Tyroller at al.), описывающая клинический случай спинальной токсоплазменной гранулемы у 7-летней кошки с прогрессирующей атаксией тазовых конечностей. При проведении КТ была обнаружена экстрадуральная масса на уровне позвонка Th9. Во время операции было выявлено однородное образование, не проникающее в костную ткань, без капсулы, рыхлой консистенции. Гистопатологически – шаровидные структуры/кистозные образования с зернистым содержимым (вероятнее всего, брадизоиты). Титр антител IgM к возбудителю токсоплазмоза был низкий, а IgG – высокий (> 1:1024). ПЦР-исследование гранулемы дало положительный результат на T. gondii. Пациенту был назначен клиндамицин в дозе 22 мг/кг 2 раза в сутки в течение 6 недель. На фоне терапии наблюдалось снижение выраженности атаксии. Повторная КТ через пять недель выявила рецидив образования. Неизвестно, был ли повторно назначен клиндамицин данному пациенту, но через 9 месяцев после операции животное было эвтаназировано вследствие прогрессии неврологического дефицита. В данной публикации отмечается, что кошка регулярно вакцинировалась и была обработана от паразитов, а также имела свободный доступ к улице6.
В 2016 году был опубликован отчет (Pfohl J. C., Dewey C. W.) о случае внутричерепной гранулемы, вызванной T. gondii, у 8-летней кошки с кластерными эпилептическими приступами. Пациенту была проведена МРТ, которая выявила наличие небольшой правосторонней контрастной массы в области обонятельной луковицы и ростральной лобной доли. Была заподозрена серповидная менингиома. Спустя 7 дней после проведения МРТ у кошки появились вялость, анорексия, гипертермия (температура – 40° C), и к противосудорожной терапии фенобарбиталом пациенту был добавлен преднизолон. Через 5 дней была проведена трансфронтальная краниотомия, в ходе которой было обнаружено желтоватое образование. Гистологическое исследование выявило лимфогистиоцитарный энцефалит, тахизоиты. Преднизолон был отменен и добавлен клиндамицин в дозе 12,5 мг/кг 2 раза в сутки. Иммуногистохимическое исследование (ИГХ) подтвердило наличие Toxoplasma gondii в образцах образования. Титры антител IgG и IgM составили 1:512 и 1:64 соответственно, что указывает на недавнее заражение или активную инфекцию. Анализы на ВИК, ВЛК у данного пациента были отрицательными. После операции у кошки наблюдались вялость, отсутствие аппетита, конъюнктивит, чиханье, гемипарез, кружение. Полностью неврологический дефицит не был устранен, а через 8 месяцев пациент был эвтаназирован из-за рецидива эпилептических приступов7.
В 2008 году был представлен отчет (Falzone C. et al.) о клиническом случае внутричерепной гранулемы у 12-летнего кота с парциальными эпилептическими приступами. За два месяца до обращения у кота наблюдалось шумное дыхание. При осмотре были выявлены угнетение, кружение влево, правосторонний гемипарез, отсутствие реакции на угрожающий жест слева и бронховезикулярные шумы при аускультации легких.
Пациенту была проведена МРТ, которая выявила объемное образование в области левой височной доли, сопровождавшееся интенсивным накоплением контраста, выраженным перифокальным отеком и масс-эффектом. На основании данных МРТ и клинической картины коту была выполнена ростротенториальная краниотомия с целью удаления образования. Цитологическое, гистологическое, иммуногистохимическое исследования подтвердили наличие организмов Toxoplasma gondii. Пациенту начали терапию клиндамицином в дозе 20 мг/кг 2 раза в сутки. Через 6 недель после операции у кота сохранялись легкие симптомы нарушения работы переднего мозга, легочные шумы разрешились, и были отменены клиндамицин и фенобарбитал. Контрольная МРТ, проведенная спустя 10 месяцев после операции, не выявила рецидива гранулемы. Спустя примерно 21 месяц после операции владелец кота повторно обратились в клинику с жалобой на угнетенное состояние питомца, продолжавшееся в течение месяца. При осмотре было установлено кружение влево, проприоцептивный дефицит и отсутствие реакции на угрозу справа. Повторная МРТ выявила рецидив образования с увеличением его объема по сравнению с результатами предыдущего исследования. Владелец животного отказался от повторного хирургического вмешательства, и была начата терапия клиндамицином, на фоне которой наблюдалось легкое улучшение состояния. Однако в течение последующих двух месяцев состояние кота ухудшалось. Пациент был вакцинирован, не имел свободного выгула, результаты тестирований на ВИК, ВЛК у него были отрицательными8.
В 2010 году был описан случай миелита (Scott A. Lindsay at al.), вызванного реактивацией спинального токсоплазмоза у 10-летнего кота. Симптомы начались с хромоты на правую грудную конечность, которая быстро прогрессировала до монопареза. Также при осмотре были установлены миоз справа и парез тазовых конечностей. Несмотря на назначение нестероидных противовоспалительных препаратов (НПВП), клиндамицина и преднизолона, положительной динамики не наблюдалось. Позднее у кота появились анорексия, поворот головы влево и неспособность передвигаться. Пациенту было проведено тестирование на ВЛК – результат отрицательный, ВИК – результат положительный (при наличии вакцинации от ВИК). Титры антител к возбудителю токсоплазмоза – IgG 1:512, IgM – отрицательные (не соответствуют активной инфекции). Титры к криптококку были отрицательные. Владельцы приняли решение об эвтаназии животного и проведении аутопсии. Посмертное гистологическое исследование выявило множественные протозойные кисты в области шейного утолщения. ИГХ исследование подтвердило наличие токсоплазмоза. Кот питался коммерческим кормом и не имел доступа к улице9.
В 2021 году был опубликован отчет (Omar V. Del Vecchio et al.) о случае многоочаговой инфильтрации центральной нервной системы Toxoplasma gondii у предположительно иммунокомпетентного 11-месячного кота (Италия)10. У молодого животного наблюдались прогрессирующие нарушения движений и многоочаговая симптоматика. МРТ выявила множественные поражения в шейном и грудопоясничном отделах спинного мозга, а также в мозговых оболочках и мозжечке. Титр IgG к возбудителю токсоплазмоза составил 640, титр IgM – 160; пороговый титр для обоих = 80. ПЦР-исследование спинномозговой жидкости на токсоплазмоз дало отрицательный результат. Пациенту был назначен клиндамицин, однако 3-недельное лечение оказалось неэффективным, состояние животного продолжало ухудшаться, и в конечном итоге было принято решение об эвтаназии. Патологоанатомическое исследование головного и спинного мозга подтвердило инфильтрацию простейшими Toxoplasma gondii. ИГХ дала отрицательный результат на инфекционный перитонит кошек, но ярко выраженный положительный результат на T. gondii. Другие инфекционные агенты не были выявлены.
Таким образом, в проанализированных клинических случаях, описанных в литературе, поражения нервной системы, вызванные токсоплазмозом, проявлялись в виде внутричерепных гранулем, спинальных гранулем, полинейропатий.
МРТ-картина обычно неспецифичная и может имитировать глиомы, менингиомы и миелиты, энцефалиты.
Диагноз ставится на основании сочетания клинических данных, серологических исследований (определение титров IgG и IgM), результатов МРТ и, при возможности, гистологического или молекулярного подтверждения (ПЦР, ИГХ). Однако низкие титры антител к возбудителю токсоплазмоза не позволяют точно определить наличие активной инфекции. Анализ литературы показывает, что не все кошки с подтвержденным токсоплазмозом имели коинфекции ВИК, ВЛК. Также зарегистрированы случаи заболевания у кошек, не имеющих свободного выгула и не употребляющих сырое мясо.
В представленном в этой статье случае клинические и нейровизуализационные данные первоначально позволяли заподозрить опухолевый процесс. Только после хирургического удаления и последующего трехэтапного исследования патологического материала (цитология, гистология и ПЦР) был поставлен окончательный диагноз «токсоплазменная гранулема головного мозга».
Терапия токсоплазмоза включает в себя применение клиндамицина (25 мг/кг в сутки в течение минимум 4–6 недель; доза может быть увеличена до 30–50 мг/кг в сутки при вовлечении в патологический процесс ЦНС) в сочетании с симптоматической терапией. Однако анализ литературы показывает, что полное выздоровление при поражении нервной системы не было зарегистрировано ни в одном случае, в связи с чем прогноз остается от осторожного до неблагоприятного.
На основании анализа клинической картины и анамнеза пациента, описанного в данной статье, можно предположить, что причина его гибели в раннем послеоперационном периоде многофакторная: скомпрометированный иммунный статус вследствие наличия как минимум двух инфекций (ВИК, токсоплазмоз), перенесенное хирургическое вмешательство, нахождение в стационаре клиники, обширное поражение мягких тканей в области латеральной поверхности грудной клетки и, как следствие, развитие синдрома системного воспалительного ответа.
Выводы:
- Церебральный токсоплазмоз у кошек может клинически и по данным МРТ имитировать опухоль головного мозга.
- Окончательная верификация диагноза возможна только при гистологическом и/или молекулярном подтверждении присутствия T. gondii.
- Даже при своевременной хирургической и противопротозойной терапии исход заболевания может быть неблагоприятным.
- Включение токсоплазмоза в список дифференциальных диагнозов при обнаружении объемных образований головного мозга у кошек имеет важное значение для выбора тактики лечения и оценки прогноза.
- Наличие коинфекции ВИК, ВЛК или иных иммуносупрессивных состояний является предрасполагающим фактором к развитию токсоплазмоза, однако наличие данных инфекций не обязательно.
- Отсутствие свободного выгула и использование промышленного корма не исключают вероятность развития токсоплазмоза.
- Dubey J.P. Toxoplasmosis of Animals and Humans. 2nd ed. CRC Press, 2010.
- Lappin M.R. Feline toxoplasmosis: interpretation of diagnostic test results. Vet Clin North Am Small Anim Pract, 2010; 40(6):1433–1446.
- Sykes J.E. Canine and Feline Infectious Diseases. St. Louis: Elsevier, 2014.
- Higgins R.J. et al. Cerebral toxoplasmosis in the cat: clinical and pathological findings. J Vet Diagn Invest, 1992; 4(4): 454–460.
- Mari L, Shelton GD, De Risio L. Distal polyneuropathy in an adult Birman cat with toxoplasmosis. J Feline Med Surg 2016; 2. DOI: 10.1177/2055116916630335.
- Florian Tyroller, Barbara Haas, et al. Toxoplasma gondii spinal granuloma in a cat. JFMS Open Rep 2023.
- Pfohl JC, Dewey CW. Intracranial Toxoplasma gondii granuloma in a cat. Journal of Feline Medicine and Surgery 2005; 7: 369–374.
- Falzone C, Baroni M, De Lorenzi D, et al. Toxoplasma gondii brain granuloma in a cat: diagnosis using cytology from an intraoperative sample and sequential magnetic resonance imaging. J Small Anim Pract 2008; 49: 95–99.
- Scott A Lindsay, Vanessa R Barrs, Georgina Child, et al. Myelitis due to reactivated spinal toxoplasmosis in a cat. Journal of Feline Medicine and Surgery (2010) 12, 818-821.
- Omar V Del Vecchio, Chiara Grande. Toxoplasma gondii multifocal central nervous system infiltration in an apparently immunocompetent cat in Italy. Vet Parasitol Reg Stud Reports 2021.
- Calero-Bernal R., Gennari S. M. Clinical toxoplasmosis in dogs and cats: an update //Frontiers in veterinary science. – 2019. – Т. 6. – С. 54.
- Lappin MR. Update on the diagnosis and management of Toxoplasma gondii infection in cats. Top Companion Anim Med 2010; 25(3): 136- 141. PMid:20937495.
- Bernsteen L, Gregory CR, Aronson LR, et al. Acute toxoplasmosis following renal transplantation in three cats and a dog. J Am Vet Med Assoc 1999; 215(8): 1123-1126. PMid:10530326.
- Last RD, Suzuki Y, ManningT, Lindsay D, et al. A case of fatal systemic toxoplasmosis in a cat being treated with cyclosporin A for feline atopy. Vet Dermatol 2004; 15(3): 194-198. PMid:15214957.
- Patton S, Legendre AM, McGavin MD, Pelletier D. Concurrent infection with Toxoplasma gondii and feline leukemia virus antibody response and oocyst production. J Vet Intern Med 1991; 5(3): 199-201. PMid:1920257.
- Heidel JR, Dubey JP, Blythe LL, Walker LL, Duimstra JR, Jordan JS. Myelitis in a cat infected with Toxoplasma gondii and feline immunodeficiency virus. J Am Vet Med Assoc. (1990) 196:316–8.
- Pena H. F. J. et al. Fatal toxoplasmosis in an immunosuppressed domestic cat from Brazil caused by Toxoplasma gondii clonal type I //Revista Brasileira de Parasitologia Veterinária. – 2017. – Т. 26. – №. 2. – С. 177-184.
- Attias M. et al. The life-cycle of Toxoplasma gondii reviewed using animations //Parasites & vectors. – 2020. – Т. 13. – №. 1. – С. 588.
- Sasai M., Yamamoto M. Innate, adaptive, and cell-autonomous immunity against Toxoplasma gondii infection //Experimental & molecular medicine. – 2019. – Т. 51. – №. 12. – С. 1-10.
- Davidson M. G. et al. Feline immunodeficiency virus predisposes cats to acute generalized toxoplasmosis //The American journal of pathology. – 1993. – Т. 143. – №. 5. – С. 1486.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург