ОЗМ (острая задержка мочи) – общий термин, применяемый для описания состояний, сопровождающихся обструкцией мочеиспускательного канала.
Актуальность проблемы
Острая задержка мочи является одной из наиболее распространенных патологий у кошек, с которой владельцы животных обращаются на амбулаторный или экстренный прием.Однако подходы к лечению пациентов с данной патологией разнятся, особенно в отношении животных, находящихся в тяжелом и критическом состоянии. Зачастую степень тяжести состояния этих пациентов недооценивается, что приводит к некорректному мониторингу и лечению.
Цель статьи: на основе анализа опубликованных данных (статей из медицинской информационно-поисковой системы Pubmed, регулярной литературы (JVECC, JASP)), а также с учетом практического опыта работы врачей ОРИТ Ветеринарной клиники доктора Сотникова выработатьунифицированный подход к пациентам с острой задержкой мочи, лечение которых осуществляется в условиях стационара.
Этиология
Острая задержка мочи является потенциально опасным для жизни проявлением заболевания нижних мочевыводящих путей у кошек. Долгое время считалось, что причиной острой задержки мочи является обструкция уретры в результате ее закупорки уролитом или слизистой пробкой (гораздо реже из-за стриктуры или неоплазии), однако результаты проведенных исследований демонстрируют, что в 50% случаев функциональная (необструктивная или идиопатическая) обструкция может играть столь же важную роль. Предполагается, что подобные состояния в уретре вызваны идиопатическим циститом кошек (англ. Feline idiopathic cystitis; FIC) – это стерильный воспалительный процесс, связанный с нейрогуморальными изменениями, возникающими в ответ на стрессовые факторы. Данный дисбаланс может приводить к развитию обструкции уретры, что связано с отеком и спазмом гладкой мускулатуры, сопровождающимися выраженным болевым синдромом1.Патофизиология
Стаз мочи приводит к повышению внутрипросветного давления в мочевом пузыре (МП) и уретре, что усиливает механическое воздействие на стенку МП. Это вызывает повреждение уротелия, проявляющееся ростом азотемии, ишемией тканей МП, некрозом его стенок и болевым синдромом. Повышенное давление ретроградно распространяется по мочеточникам к почкам, что приводит к снижению функции клубочкового аппарата. В результате развивается обструктивная нефропатия, характеризующаяся снижением скорости клубочковой фильтрации (СКФ) и метаболическим ацидозом. Гипоперфузия почек усугубляется, что вызывает некроз почечных канальцев и острое повреждение почек (ОПП)1-3.Анамнез и клинические признаки 1-3,5
При классическом течении заболевания отмечаются следующие клинические признаки:- отсутствие мочеиспускания более 12 часов;
- непродуктивные позывы к мочеиспусканию;
- странгурия, проявляющаяся вокализацией в процессе попыток мочеиспускания;
- увеличение живота в объеме за счет перерастяжения мочевого пузыря;
- выраженная абдоминальная болезненность, особенно при пальпации в проекции почек;
- в случае обструкции дистальных участков уретры сгустком или уролитом может наблюдаться воспаление полового члена;
- апатия, анорексия.
- Электролитные нарушения: гиперкалиемия и гиперфосфатемия могут усугублять степень тяжести состояния пациента.
- Кардиологические проявления: брадикардия и нарушение внутрисердечной проводимости.
- Гиповолемия: тяжелая степень обезвоживания проявляется снижением тургора кожи, ухудшением качества кожных покровов и шерсти, сухостью и липкостью слизистых оболочек, а также западением глазных яблок. Параллельно наблюдается снижение периферической перфузии, что проявляется бледностью слизистых оболочек, изменением частоты сердечных сокращений, увеличением скорости наполнения капилляров, ослаблением пульса при пальпации крупных артерий.
- Артериальная гипотензия и снижение церебрального кровотока: снижение системного артериального давления и, как следствие, ухудшение мозгового кровообращения могут привести к снижению уровня сознания вплоть до коматозного состояния.
- Метаболический ацидоз: респираторная компенсация проявляется тахипноэ, что может привести к развитию респираторного алкалоза.
Госпитализация
После поступления пациента в ОРИТ основной задачей врача интенсивной терапии является оказание неотложной медицинской помощи с целью снижения рисков развития следующих жизнеугрожающих состояний: болевой синдром, гиповолемия, гиперкалиемия, гипокальциемия, уремия, метаболический ацидоз.Болевой синдром и аналгоседация1-3,5,8
В основе развития болевого синдрома у пациентов с острой задержкой мочи лежит механическая либо физиологическая обструкция мочеиспускательного канала с последующим перерастяжением стенок мочевого пузыря и развитием гидронефроза.С целью коррекции болевого синдрома рекомендовано применение мультимодальной анальгезии. До момента стабилизации гемодинамических параметров пациента рекомендовано применение таких опиоидных препаратов, как фентанил, морфин, буторфанол (при наличии соответствующей лицензии на работу с наркотическими средствами и психотропными веществами, а также при условии наличия в самой клинике данных лекарственных средств). Помимо опиоидных препаратов, может быть рациональным применение NMDA-антагонистов, таких как кетамин.
В тех случаях, когда у клиники отсутствует лицензия на деятельность, связанную с оборотом сильнодействующих, наркотических и психотропных веществ, можно рассмотреть вариант применения комбинированных препаратов, содержащих тилетамин и золазепам, или использование дексмедетомидина.
Решение о применении дексмедетомидина должно быть принято с особым вниманием, исходя из оценки гемодинамического статуса пациента, а также с точки зрения соотношения потенциальной пользы и потенциального вреда от использования данного препарата.
Помимо этого, может быть рациональным применение трамадола. Несмотря на то что включение данного препарата в терапевтический протокол лечения кошек является предметом регулярных споров между врачами интенсивной терапии, при отсутствии альтернативы, на мой взгляд, это представляется возможным.
С целью дополнительной седации (при необходимости) можно рассмотреть использование ацепромазина, тразодона и габапентина.
Пациентам с острой задержкой мочи категорически противопоказано применение нестероидных противовоспалительных препаратов (НПВП) в связи с их выраженными нефротоксическими свойствами. Рассматривать возможность использования НПВП можно только после регидратации пациента, нормализации темпа диуреза и разрешения азотемии.
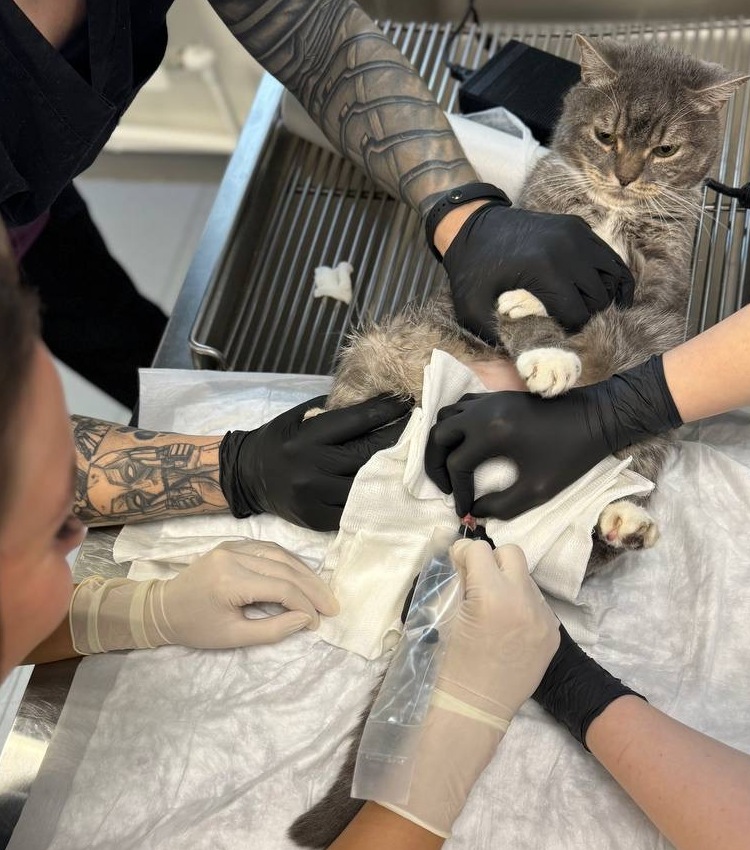
После первичной анальгезии следует устранить непосредственную причину болевого синдрома – перерастяжение стенок мочевого пузыря. Для этого рекомендовано выполнение декомпрессионного цистоцентеза с целью опорожнения мочевого пузыря и снижения давления в мочевыводящих путях, что приводит к облегчению болевого синдрома.
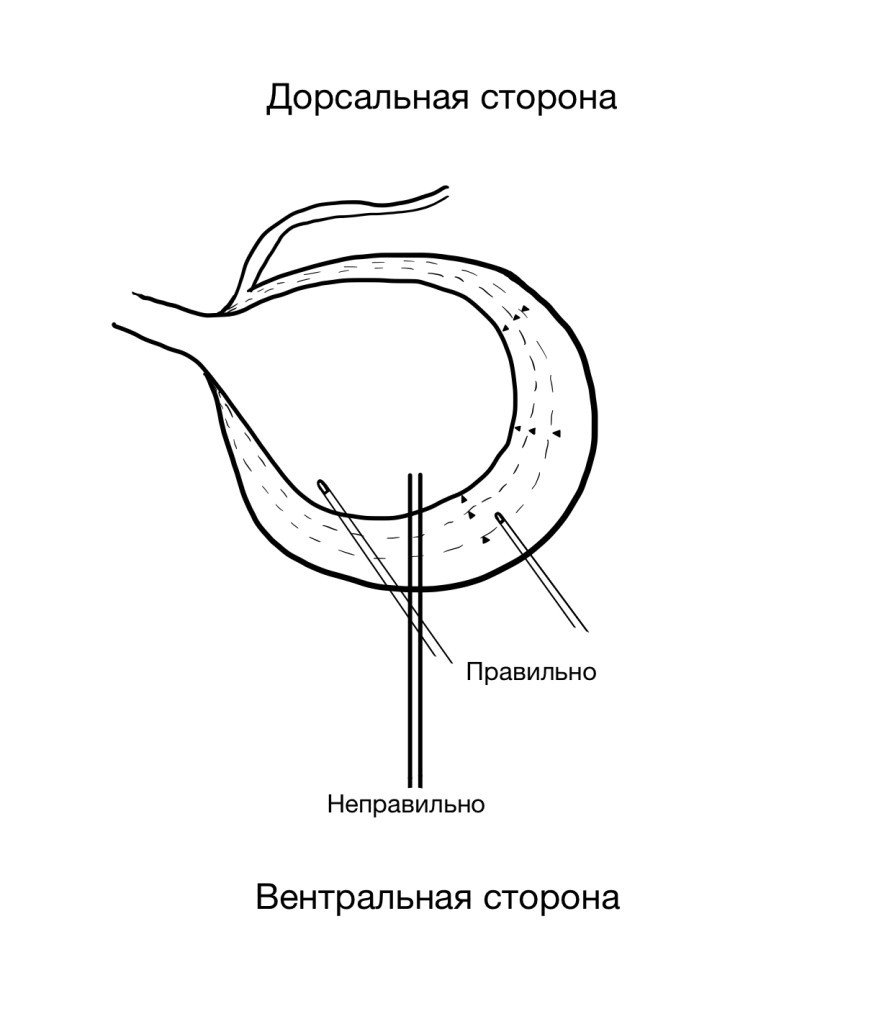
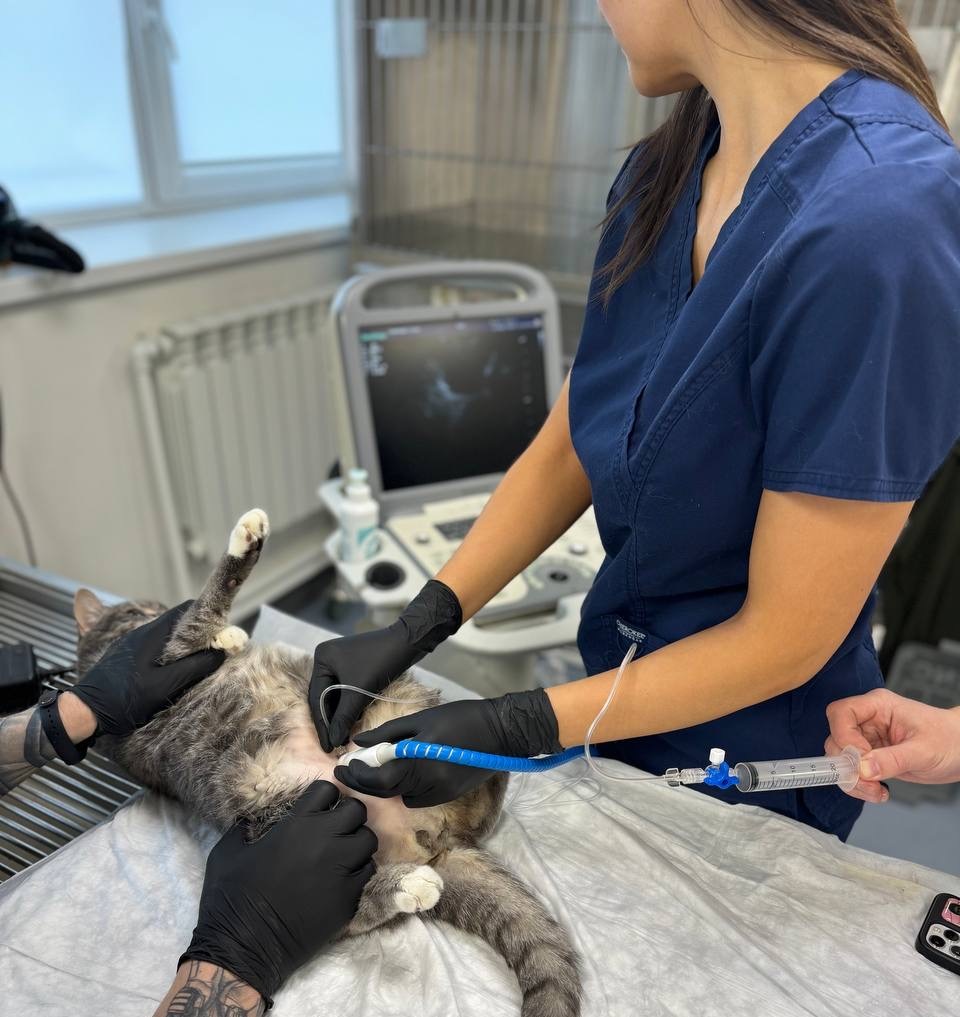
Во время проведения данной процедуры в мочевой пузырь вводится игла диаметром 22G с заранее подключенной магистралью длиной 150 см и шприцом объемом 20 мл для последующего опорожнения мочевого пузыря. Пункция производится в область шейки мочевого пузыря, иглу следует направлять каудально (рис.1-3).
При проведении декомпрессионного цистоцентеза, несмотря на экстренность процедуры и кажущуюся простоту ее выполнения, следует строго соблюдать методы асептики и антисептики.
Установку уретрального катетера пациентам (за исключением животных, находящихся в терминальном состоянии) мы рекомендуем выполнять с применением эпидуральной анестезии сразу после стабилизации гемодинамики, процедуру необходимо проводить так быстро, насколько это возможно.
Коррекция гиповолемии1,3
Большинство ветеринарных врачей с целью коррекции гиповолемии рекомендуют применение сбалансированных кристаллоидных растворов (лактатный раствор Рингера, стерофундин и др.). Несмотря на наличие в составе данных растворов калия (5 и 4 ммоль/л соответственно), введение их в больших объемах с параллельным разрешением обструкции мочевыделительной системы приводит к снижению как относительного, так и абсолютного уровня калия в организме. Однако на текущий момент (на основании анализа сроков госпитализации пациентов и влияния на исход) отсутствуют убедительные доказательства преимущества применения сбалансированных кристаллоидных растворов в сравнении с обычным физиологическим раствором (0,9%-ный раствор натрия хлорида). По этой причине выбор кристаллоидного раствора остается на усмотрение врача-клинициста.При расчете скорости инфузии следует учитывать следующие компоненты:
- дефицитный объем;
- поддерживающий объем;
- потери, обусловленные постобструктивным диурезом;
- иные потери (рвота, тахипноэ, потери в третье пространство).
В нашем отделении мы пользуемся следующими упрощенными формулами (конечный результат исчисляется в миллилитрах):
ДО = масса тела (кг) × % дегидратации × 8.
ПО = масса тела (кг) × 30 + 70
Особую и порой решающую роль при расчете объема инфузионной терапии для пациентов с острой задержкой мочи играет учет потерь жидкости, обусловленный постобструктивным диурезом.
По нашим наблюдениям, а также по данным ряда литературных источников, средний темп постобструктивного диуреза может составлять 5–20 мл/кг/ч1,4,5. Считается, что он возникает вследствие накопления в крови осмотически активных веществ или резистентности вазопрессиновых рецепторов в почках к воздействию антидиуретического гормона3,4,5.
Клинический пример
Пациент: кот с идеальной массой тела 5 кг поступил в ОРИТ с острой задержкой мочи в тяжелом состоянии, обусловленном в том числе гиповолемией.
Врачом на приеме был определен дефицит гидратации – 10%:
ДО = 5 × 10 × 8 = 400 мл
ПО = 5 × 30 + 70 = 220 мл
Суммарный суточный объем составлял 620 мл
При наличии признаков гиповолемии рекомендовано восполнять дефицитный объем в течение первых 6 часов с момента госпитализации. Соответственно, базовая скорость инфузии в первые шесть часов составит минимум 400/6 = 66 мл/ч.
Однако при наличии умеренной потери, обусловленной постобструктивным диурезом (например,10 мл/кг/ч), данный пациент будет терять не менее 50 мл/ч. Следовательно, водный баланс за первые 6 часов вместо + 400 мл составит + 96 мл без полноценного восполнения общего циркулирующего объема крови.
В случае наличия более выраженного постобструктивного диуреза отсутствие адекватного расчета скорости инфузионной терапии и вовсе может привести к манифестации признаков гиповолемии, метаболического ацидоза и стать причиной гибели пациента.
Из вышеизложенного следует, что скорость инфузии для данного пациента в первые шесть часов должна приблизительно составить 116 мл/ч с коррекцией на потери с мочой.
Спустя 6 часов от старта инфузии следует произвести переоценку степени дегидратации и рассчитать новый ДО, скорректировав оставшийся дефицит в течение последующих суток с обязательным строгим учетом темпа постобструктивного диуреза. В последующие сутки (вплоть до нормализации темпа диуреза) следует придерживаться нулевого водного баланса, соответственно, суточный объем инфузии с учетом персонального потребления воды пациентом должен состоять
из ПО + потери, обусловленные постобструктивным диурезом.
Перерасчет потерь мочи следует производить каждые 3–4 часа.
Разрешается постобструктивный диурез обычно в течение 2–5 суток.
Коррекция гипокалиемии1-3,7,8
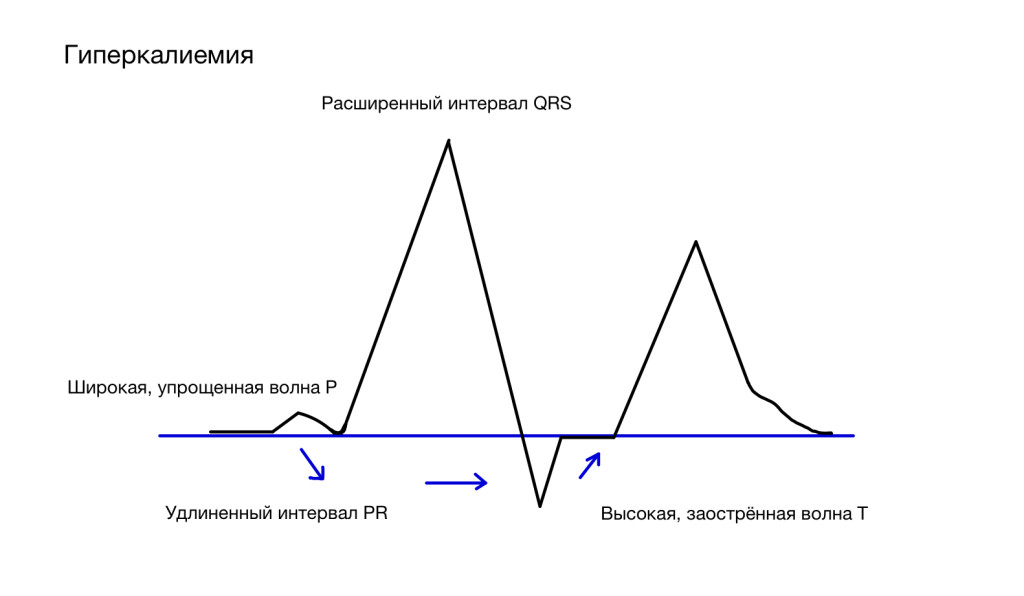
Основным методом коррекции гипокалиемии является устранение ее причины – восстановление адекватного оттока мочи путем разрешения обструкции или уретральной катетеризации (рис. 4).При оценке клинической значимости гиперкалиемии рекомендовано ориентироваться на данные ЭКГ. Характерными для гиперкалиемии симптомами являются снижение амплитуды или отсутствие зубца P, расширение комплекса QRS, а также высокий «пиковый» зубец Т. По мере усугубления гиперкалиемии ЭКГ-признаки могут прогрессировать до остановки предсердий, желудочковой тахикардии и фибрилляции желудочков или асистолии.
Разрешение обструкции и восстановление адекватного оттока мочи являются основными методами достижения задачи разрешения гиперкалиемии, однако этот процесс требует времени.
Если у пациента наблюдаются ЭКГ-признаки гиперкалиемии, рекомендуется немедленное вмешательство, а именно: медленное внутривенное (в течение 1–2 минут) введение кальция глюконата в дозе 100–150 мг/кг. Кардиопротективный эффект от введения кальция глюконата длится около 40–60 минут. При необходимости болюс можно повторить.
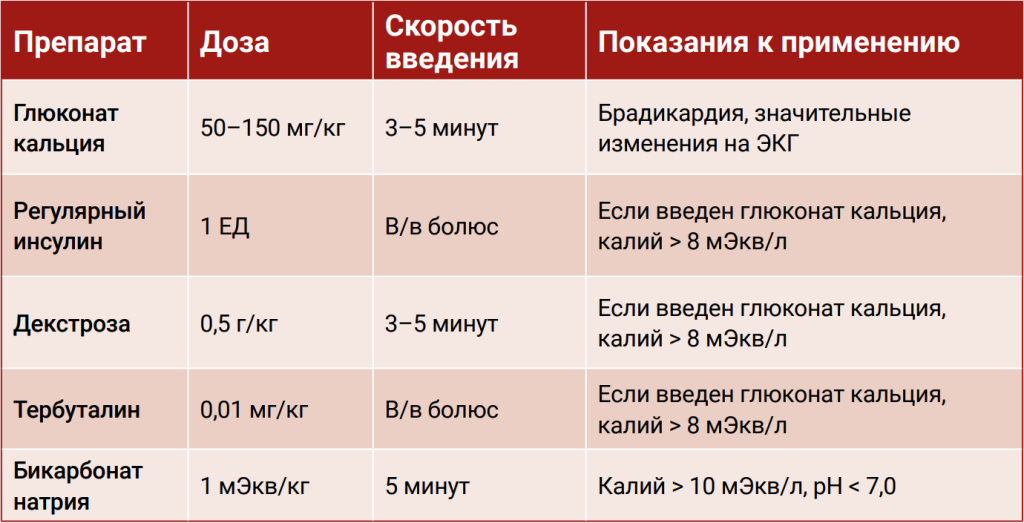
В случае отсутствия эффекта от болюсного введения кальция глюконата рекомендовано применение ИПС глюкозо-инсулиновой смеси в дозе 0,25–1,0 ЕД/кг инсулина на каждые 1–2 г/кг глюкозы.
Эти и другие методы коррекции гиперкалиемии указаны в таблице 13.
Коррекция гипокальциемии7-9
По данным одного из исследований, гипокальциемия наблюдается у 75% котов, владельцы которых обратились на прием с симптомами острой задержки мочи у своих питомцев9. Предполагается, что клинически значимая гипокальциемия вызвана преимущественно связыванием ионизированного кальция большим количеством фосфатов.Коррекция гипокальциемии заключается во введении 100–150 мг/кг кальция глюконата. Симптомы, как правило, нивелируются сразу после введения.
Коррекция уремии
Уремия играет решающую роль в развитии метаболического ацидоза и уремической энцефалопатии, а также постобструктивного диуреза, так как мочевина является одним из трех основных осмотически активных компонентов плазмы.Коррекция уремии заключается в восстановлении оттока мочи, устранении гиповолемии, нормализации почечной перфузии и адекватной инфузионной терапии, описанной выше.
Коррекция метаболического ацидоза7,10
рН – одна из главных гомеостатических констант живого организма. Вследствие нарушения функции почек как метаболического компонента кислотно-щелочного баланса организма происходит задержка свободных ионов водорода, приводящая к смещению рН в сторону ацидоза. Виной тому – накопление в плазме пациентов слабых кислот и рост разницы сильных ионов.Основные методы коррекции метаболического ацидоза у данной категории пациентов – это восстановление оттока мочи и инфузионная терапия с применением сбалансированных кристаллоидных растворов.
В случае критического снижения рН < 7,2 может быть рациональным применение натрия бикарбоната в дозе 2–5 мЭкв/кг, что соответствует 4–10 мл/кг массы тела до достижения конечных точек (pH > 7,2).
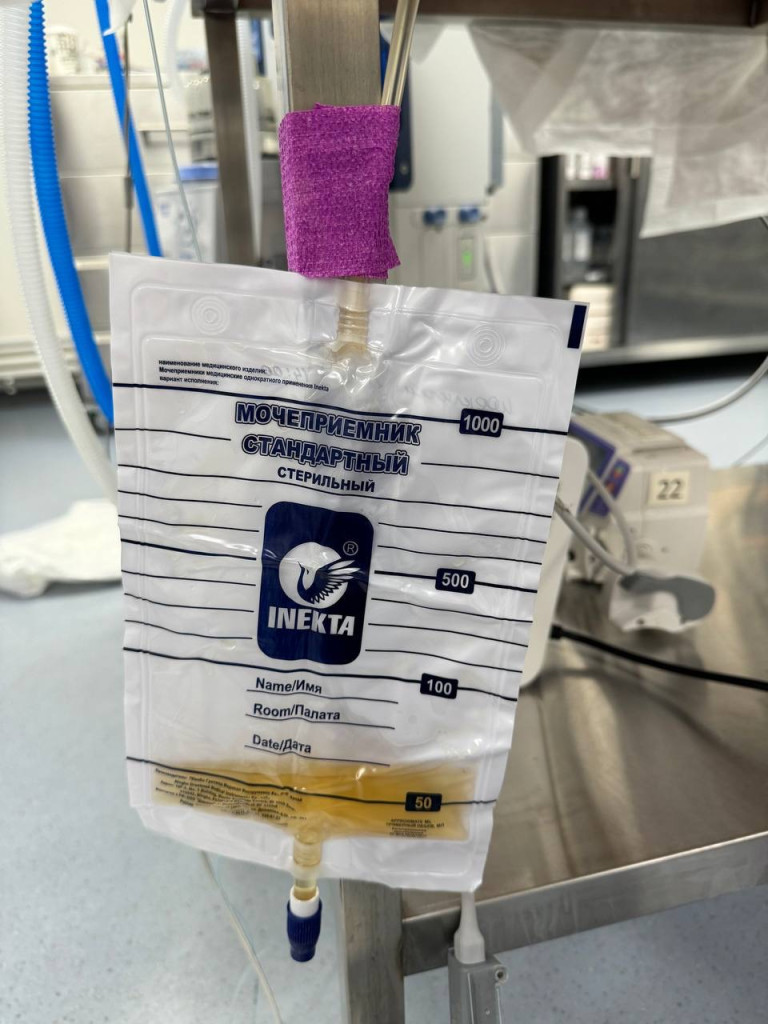
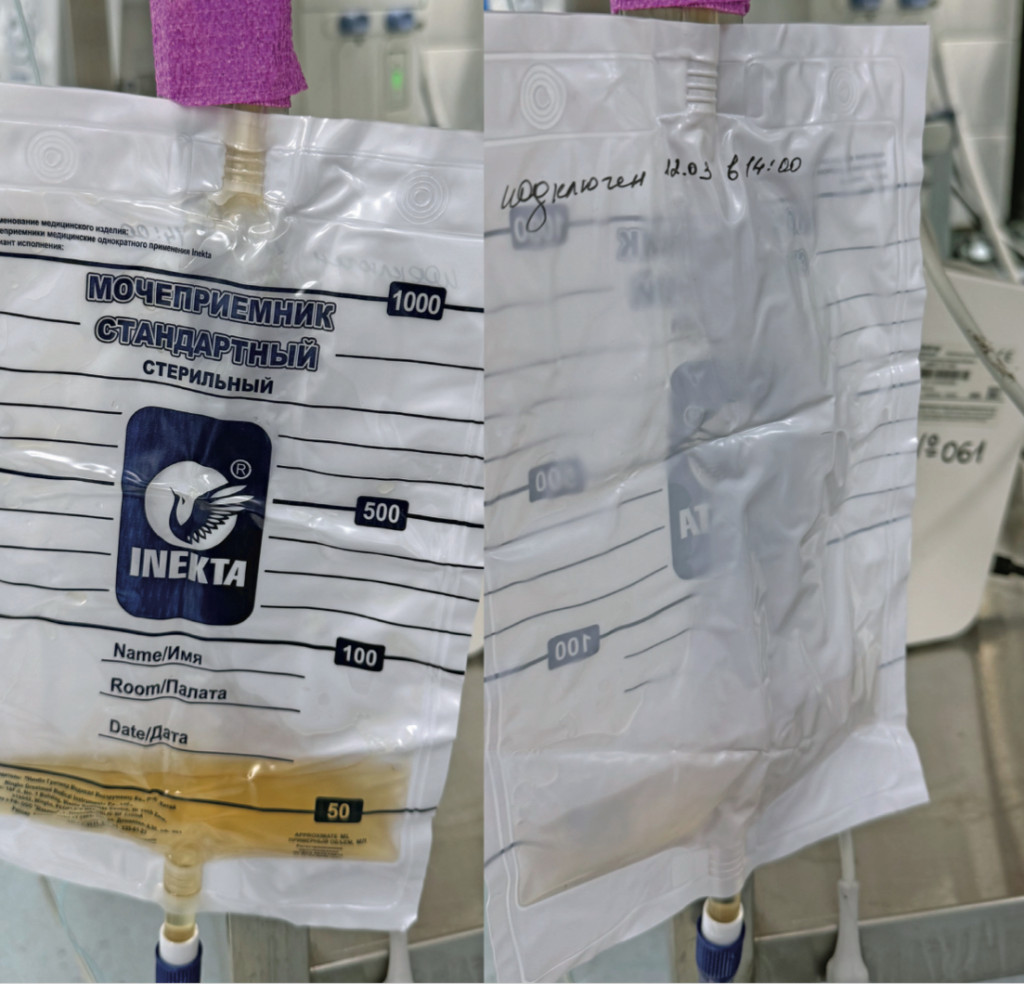
Сразу после стабилизации гемодинамических параметров параллельно с выполнением вышеописанных процедур рекомендовано проведение катетеризации уретры5,6,8. Цель установки уретрального катетера заключается в восстановлении и поддержании адекватного оттока мочи, а также подсчете темпа диуреза (рис. 5).
Несмотря на наличие рисков, связанных с уретральной катетеризацией (ятрогенная травма уретры и мочевого пузыря, ретроградное занесение инфекции), данную процедуру следует рутинно проводить пациентам с симптомами острого повреждения почек, поступающим в ОРИТ. Пациентам, находящимся в терминальном состоянии, допустимо проведение уретральной катетеризации без седации. Всем остальным пациентам должна быть выполнена седация (протокол седации; табл. 25).
Выбор анестезиологического протокола осуществляется в зависимости от наличия в клинике наркотических средств и психотропных веществ, а также с учетом гемодинамического статуса пациента.
После седации мы рекомендуем рутинное выполнение эпидуральной анестезии (ЭА). Помимо продленного анальгетического эффекта при применении бупивакаина, ЭА позволяет расслабить гладкую мускулатуру и облегчить введение уретрального катетера.
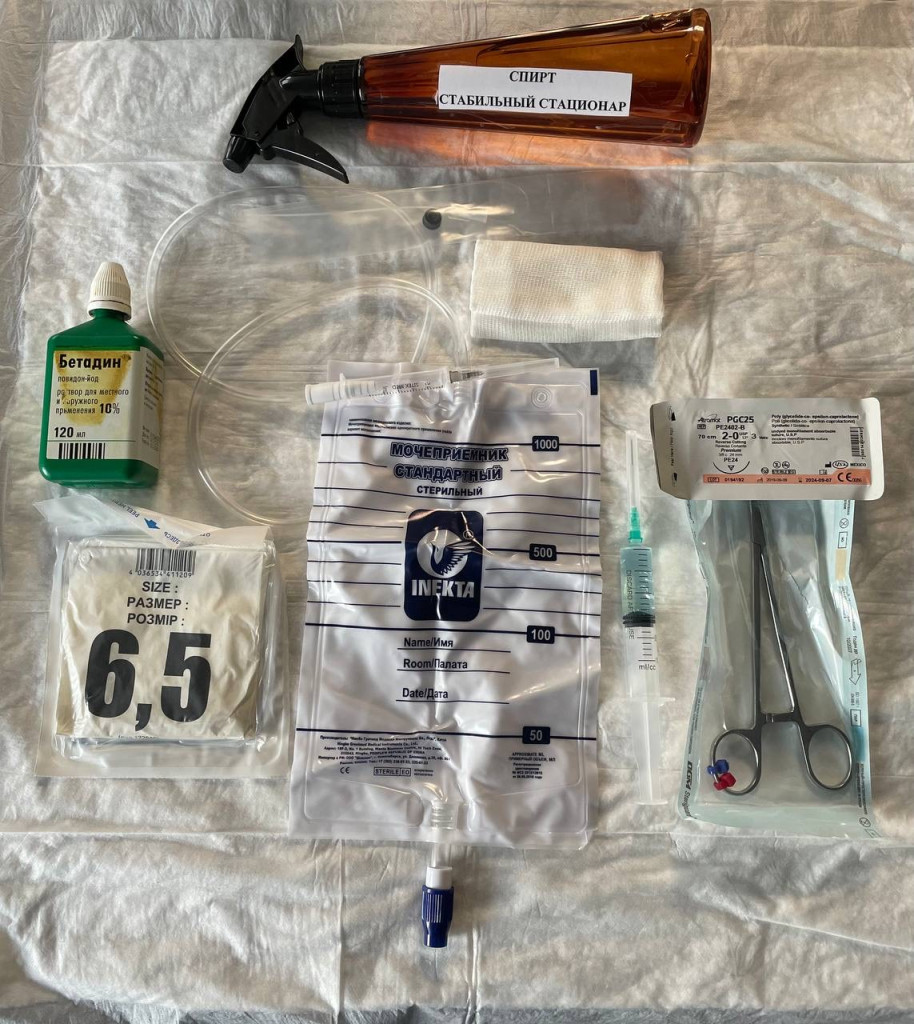
Уретральный катетер должен быть установлен строго с соблюдением всех правил асептики и антисептики, с должной подготовкой операционного поля и соблюдением стерильности (рис. 6, 7).
При механической обструкции уретры (уролитом или слизистым сгустком) возможно проведение ретроградной уретрогидропульсии. Также может быть рациональным применение техники, при которой ассистент пережимает простатическую часть уретры через прямую кишку, пока дистальный отдел уретры наполняется солевым раствором, а затем резко ослабляет нажим, отпуская палец. Данная техника может позволить промыть уролит/сгусток в мочевой пузырь путем создания более высокого давления в уретре.
После установки уретральный катетер должен быть немедленно присоединен к мочеприемнику. Смену мочеприемника и разгерметизацию системы необходимо производить исключительно по показаниям. Мочеприемник впоследствии можно использовать для рутинного подсчета темпа диуреза, однако мы рекомендуем производить более точный подсчет путем сливания мочи и ручного подсчета с помощью шприца.
В дальнейшем критериями для удаления уретрального катетера являются следующие факторы:
- стабилизация гемодинамических параметров;
- восстановление темпа диуреза;
- разрешение уремии;
- разрешение гиперкалиемии.
Выводы
Несмотря на то что острая задержка мочи является одной из наиболее распространенных патологий в рутинной практике врача общего приема и редко приводит к гибели животных, практикующим врачам следует более внимательно относиться к стабилизации состояния этих пациентов.При работе с ургентными пациентами необходимо уделять особое внимание коррекции таких состояний, как выраженный болевой синдром, гиповолемия и гемодинамические нарушения, метаболический ацидоз, гиперкалиемия, гипокальциемия и уремия.
Список литературы:
- Clinical Small Animal Internal Medicine by David Bruyette (editor), 2020, John Wiley & Sons, Inc.
- Handbook of Canine and Feline Emergency Protocols by Maureen McMichael (editor), 2014, John Wiley & Sons, Inc.
- Kenneth J. Drobatz, Kate Hopper, Elizabeth Rozanski, Deborah C. Silverstein. Textbook of Small Animal Emergency Medicine, 2019, John Wiley & Sons, Inc.
- Small animal emergency care. Quick reference guide, 2017, Grupo Asís Biomedia, S.L.
- Edward S. Cooper. Controversies in the management of feline urethral obstruction, 2015.
- Angela K. O'Hearn, Bonnie D. Wright. Coccygeal epidural with local anesthetic for catheterization and pain management in the treatment of feline urethral obstruction, 2011.
- Justine A. Lee, Kenneth J. Drobatz. Characterization of the clinical characteristics, electrolytes, acid-base, and renal parameters in male cats with urethral obstruction, 2003.
- Clarke D. L. Feline ureteral obstructions Part 1: medical management, 2018.
- Drobatz K. J., 1. Hughes D. Concentration of ionized calcium in plasma from cats with urethral obstruction, 1997.
- Stewart P. A. How to Understand Acid-Base. New York: Elsevier, 1981.



 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург