Сравнительные характеристики
Автор: Сейлиев Д. А., ветеринарный врач-хирург, онколог Ветеринарной клиники Сотникова, г. Санкт-Петербург.
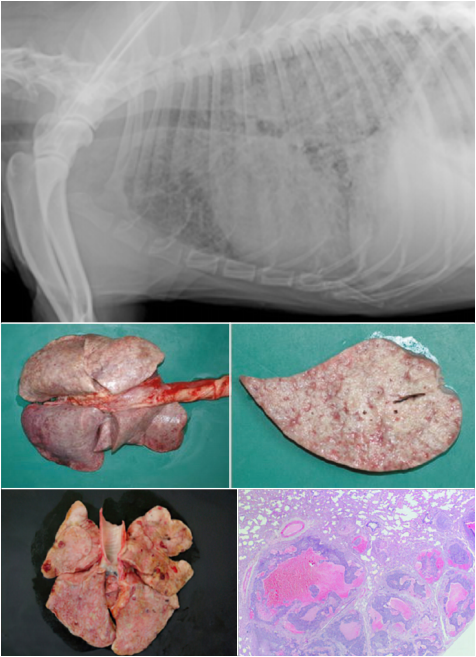
Первичные новообразования легких встречаются у кошек и собак не так часто, как вторичные метастатические поражения легочной ткани (вторичные или метастатические новообразования легких, фото 3). По этой причине речь в статье пойдет именно о первичных новообразованиях, но с разными клиническими проявлениями.
Первичные новообразования можно подразделить на две большие группы:
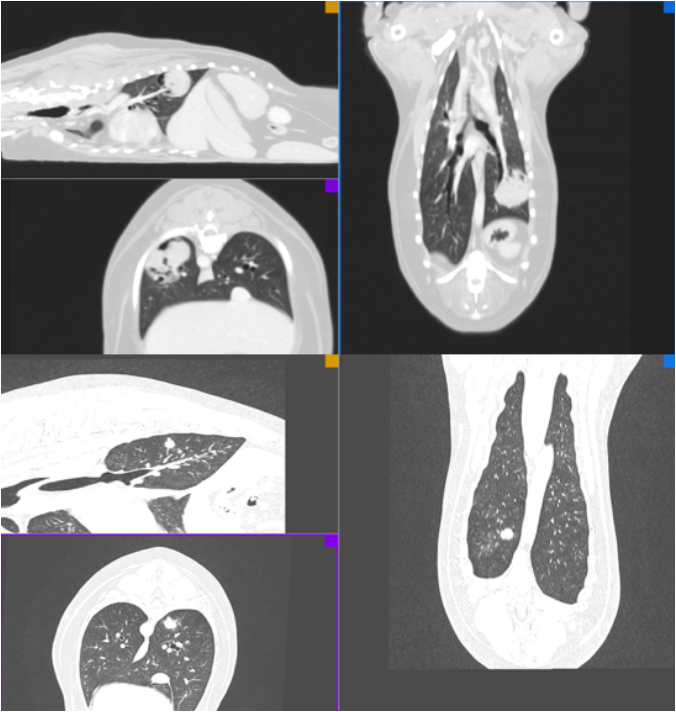
- солитарные (сОлидные) новообразования легких (фото 1);
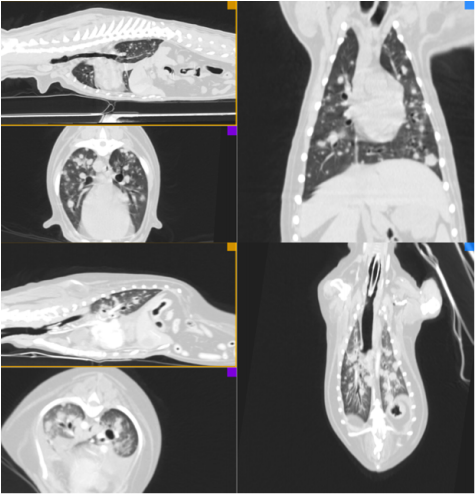
- диссеминированные новообразования легких, которые встречаются крайне редко и зачастую ошибочно диагностируются и лечатся как бронхопневмонии (фото 2).
Заболеваемость первичным раком легких у мелких домашних животных составляет менее 1% случаев1-4. Показатели заболеваемости у собак варьируются от 4,2 до 15 случаев на 10 000 собак в год в Соединенных Штатах Америки5,6. Средний возраст домашних собак, у которых диагностируются первичные опухоли легких, составляет около 5 лет.
Первичные опухоли, как правило, выявляются рентгенологически в виде хорошо очерченной одиночной массы на периферии каудальных долей легких. Все первичные опухоли легких с внутренними воздушными бронхограммами имеют бронхоцентрическое происхождение. Бронхи обычно сужены, смещены и часто закрыты опухолью. В среднем 95% опухолей единичные, но также встречаются и мультифокальные формы новообразований легких. Большинство одиночных опухолей хорошо очерчены, расположены в центральной части к периферии легкого или в каудальной доле. Основная масса первичных опухолей легких имеет незначительное или умеренное гетерогенное контрастное усиление при введении рентгеноконтрастного вещества. Внутренняя минерализация встречается у 8%, а трахеобронхиальная лимфаденопатия выявляется у 12% собак. При КТ-исследовании единичные, хорошо очерченные бронхоцентрические массы с внутренними воздушными бронхограммами согласуются с первичной опухолью легких у собак.
Патогенез
Первичные новообразования легких могут возникать из любой ткани легкого, но чаще всего – из эпителия дыхательных путей или паренхимы альвеол. Новообразования, сформированные из эпителия крупных бронхов, обычно располагаются рядом с воротами или корнем легкого, тогда как опухоли, происходящие из паренхимы, имеют тенденцию располагаться на периферии. Однако самые последние руководящие принципы ВОЗ призывают классифицировать новообразования легких у домашних животных по гистологическому типу, а не по месту происхождения. Приблизительно 85% опухолей легких у собак являются бронхоальвеолярными по происхождению, тогда как аденокарцинома, аденосквамозная и плоскоклеточная (SCC) карциномы вместе составляют оставшиеся 13–15% первичных опухолей легких7,8, при этом наиболее распространенной из них является аденокарцинома (от 60% до 70%). Авторы отмечают предрасположенность к возникновению первичных опухолей легких у следующих пород собак: боксер, доберман, австралийская овчарка, ирландский сеттер и бернский зенненхунд1,8.По данным зарубежных источников, первичная опухоль легких обнаруживается у пациентов случайно во время обычного гериатрического скрининга1,7,11. Однако в большинстве случаев такие находки являются прямым следствием скрупулезной работы с пациентом – оценки его клинического состояния и выявления клинических признаков в процессе сбора анамнеза. До 30% случаев первичных опухолей легких диагностируются без наличия каких-либо клинических признаков.
Клиническим признаком у собак с легочной неоплазией является кашель, отмечающийся у 52–93% пациентов1,11-14.
Другие клинические признаки включают одышку (от 6 до 24%), летаргию (от 12 до 18%), анорексию (13%), потерю веса (от 7 до 12%), кровохарканье (от 3 до 9%) и хромоту. Вероятно, хромота является вторичной по отношению к гипертрофической остеопатии (4%)11-13. Гипертрофическая остеопатия – это паранеопластический синдром (ПНС), который чаще всего ассоциируется с первичными и метастатическими опухолями легких, хотя другие злокачественные и незлокачественные заболевания также могут приводить к его возникновению13,15-19. Данный паранеопластический синдром характеризуется выраженной периостальной реакцией, которая возникает вследствие диффузных изменений, как правило, поражающих дистальные отделы длинных трубчатых костей. Клиническое проявление хромоты может улучшиться после проведения оперативного вмешательства, направленного на полное удаление новообразования легочной ткани (или любого другого), в результате которого сформировался данный ПНС15,18.
Методы диагностики
Клинические лабораторные исследованияРезультаты общего клинического (Complete Blood Count, CBC) и биохимического анализов крови не могут дать врачу достоверную информацию о наличии опухолевого процесса в легких, но в ряде случаев при гнойно-некротическом распаде новообразования могут повышаться уровни лейкоцитов, нейтрофилов, моноцитов.
Плевральный выпот в грудной полости у собак встречается реже, чем у кошек. Если в процессе диагностики отмечается наличие выпотной жидкости, то в обязательном порядке с помощью торакоцентеза осуществляется отбор ее образца, который отправляют в лабораторию для проведения оценки состава.
В качестве методов диагностики неоплазии легких рекомендованы бронхоальвеолярный лаваж (БАЛ) и транстрахеальные смывы.
Из 14 случаев БАЛ был определяющим в восьми, сомнительным – в четырех и бесполезным – в двух случаях20. Транстрахеальные смывы были менее успешными: в одном исследовании ни у одной из шести собак с подтвержденной первичной легочной неоплазией БАЛ не дал положительного результата в отношении обнаружения опухолевых клеток в смывах20.
Визуальная диагностика
Большинство опухолей легких диагностируется на рентгенограммах грудной клетки. В двух больших исследованиях с участием 277 собак у 83% животных неоплазия легких была диагностирована с помощью рентгенограмм грудной клетки11,13. У собак с первичными опухолями легких в 67–91% случаев на рентгенограммах грудной клетки будут выявляться как единичные, так и мультифокальные новообразования11.Локализация и количество опухолей в легких оценивались в нескольких исследованиях1,12,13. При проведении рентгенологического исследования 210 собак с первичными новообразованиями легочной ткани точная локализация опухолей была определена в 191 случае13. Из общего количества исследованных собак новообразования были обнаружены в одной доле легкого у 53,8% животных и были интерпретированы как мультифокальные новообразования легких у 37,1% животных13.
Лечение
При первичных опухолях легких хирургическое лечение является методом выбора, причем тип хирургического вмешательства зависит от предпочтений клинициста, но существуют общие критерии, определяющие выбор хирургической тактики лечения. При наличии односторонних опухолей может быть выполнена паракостальная торакотомия или срединная медиальная стернотомия. Эндоскопическая лобэктомия рассматривается только при обнаружении новообразований, располагающихся на периферии легкого, поскольку в этом случае они будут легко интерпретироваться врачом-эндоскопистом.Если опухоли являются билатеральными (то есть поражают левые и правые доли легких) и целью хирургической манипуляции будет удаление всех новообразований, следует выполнять срединную стернотомию. Однако использование данной методики для лечения пациентов с билатеральным поражением легких все еще подлежит обсуждению.
В литературе описаны как частичные, так и полные лобэктомии долей легких, и выбор методики будет основываться на локализации опухоли. В основном пациентам с опухолевыми поражениями требуется проведение полной лобэктомии легких, однако частичная лобэктомия легкого может быть вариантом для небольших опухолей, расположенных на периферии пораженной доли легкого. Частичные и полные лобэктомии легких, как правило, выполняются либо методом наложения швов, либо с использованием хирургического степлера. Пневмонэктомия (полное удаление легкого) может быть выполнена только при наличии соответствующих показаний21.
Биопсия лимфатических узлов рекомендуется в качестве инструмента постановки комплексного диагноза, поскольку метастатическое поражение лимфатических узлов значительно влияет на показатели медианы выживаемости14. Биопсию лимфатических узлов относительно легко выполнить с помощью паракостальной торакотомии, гораздо более сложной задачей является выполнение биопсии при стернальной торакотомии.
При наличии поражений лимфатических узлов рекомендуется использование протоколов противоопухолевой терапии.
Протоколы химиотерапии на основе цисплатина в гуманной медицине считаются стандартными для пациентов, получающих противоопухолевую терапию в формате адъювантной или паллиативной помощи22. Об эффективности химиотерапевтического лечения опухолей легких у домашних животных известно немного, однако на основании имеющейся информации можно сделать вывод о том, что химиотерапия в большинстве случаев была нецелесообразной.
Ранние клинические испытания, оценивавшие безопасность и эффективность применения доксорубицина у собак, включали несколько пациентов с папиллярными аденокарциномами легких (поддающимися оценке), у которых отмечалась прогрессия заболевания.
У трех собак с аденокарциномой легкого, которых лечили митоксантроном, ответов на терапию получено не было. Улучшения отмечались у двух собак, для лечения которых был назначен виндезин, в то время как у других двух собак, получавших комбинацию виндезина и цисплатина, наблюдалось уменьшение опухолевых масс более чем на 50%12. Лечение винорелбином привело к частичным ответам у двух из семи собак с неоперабельной бронхоальвеолярной карциномой11. У трех собак с небольшими, но множественными очагами (при условии незначительных поражений легких) лечение адъювантным винорелбином продлило время выживания до 113, 169 и более 730 дней 42. Фармакокинетические исследования, проведенные на людях, показали, что лечение винорелбином приводит к 300-кратному повышению концентрации препарата в легких по сравнению с плазмой, это в 3,4 и 13,8 раза выше, чем концентрации в легких виндезина и винкристина соответственно12.
На основании полученных частичных ответов у собак и фармакокинетических данных у людей лечение винорелбином или цисплатином представляется наиболее перспективным.
Описаны способы доставки химиотерапевтических препаратов и цитокинов методом аэрозолей, которые хорошо переносится животными с первичной или метастатической неоплазией легких. Полные и частичные ответы были описаны у собак, получавших ингаляционную терапию при лечении метастатических опухолей, тогда как у собак с первичными опухолями легких сообщалось о стабильном или прогрессирующем заболевании13,14.
Также имеются публикации об использовании схем метрономной химиотерапии с применением циклофосфамида, пироксикама и талидомида36.
Было доказано, что лечение низкомолекулярными ингибиторами тирозинкиназы (TKI) - таргетными противоопухолевыми препаратами, является результативным для различных подгрупп пациентов с немелкоклеточным раком легких (non-small-cell lung cancer; NSCLC). Подобные методы лечения собак с данным заболеванием еще предстоит тщательно изучить. Благодаря недавнему появлению ингибиторов тирозинкиназных рецепторов (TKI) – тоцераниба (Palladia) и маситиниба (Kinavet), предназначенных для терапии онкологических больных в ветеринарии, использование указанных препаратов для лечения пациентов с опухолевыми поражениями легких в дальнейшем может иметь большую доказательную базу. В одном из исследований был сделан вывод о том, что монотерапия тоцеранибом у одной собаки с первичным раком легких, включенной в исследование, привела к стабилизации заболевания более чем на 10 недель29.
Пациенты со злокачественными интраплевральными поражениями могут хорошо отвечать на системную противоопухолевую терапию, внутриплевральную химиотерапию или комбинацию вышеперечисленных методов (при этом используются цисплатин, карбоплатин или митоксантрон).
Развитие радиационной терапии в медицине было основана на том, что опухоли чаще всего неоперабельны22. Локальное облучение местнораспространенного немелкоклеточного рака легких (НМРЛ) у людей традиционно рекомендовано, но в настоящее время является источником противоречий. Такие технологии, как лучевая терапия с модулированной интенсивностью (intensity modulated radiation therapy; IMRT), гамма-нож или томотерапия, теперь могут использоваться для обеспечения более точного направления излучения, сводя к минимуму воздействие на окружающие здоровые ткани, особенно при совместном использовании с методами дыхательной вентиляции или задержки дыхания. Применение данных методов для лечения ветеринарных пациентов в настоящее время становится доступным, но пока еще требует детального изучения у собак и кошек с опухолями легких.
Интервенционная онкология – это область интервенционной радиологии, которая занимается диагностикой и лечением рака и связанных с ним проблем при помощи использования целевых минимально инвазивных процедур, выполняемых под визуальным контролем. Интервенционные методы лечения первичной легочной неоплазии не были описаны в ветеринарной литературе, однако в медицине существует несколько терапевтических подходов37-40, применяемых, как правило, для лечения пациентов с признаками легочной метастатической болезни или пациентов, которым противопоказана операция из-за наличия сопутствующих заболеваний или неоперабельной опухоли легких. Перед тем как использование указанных методов у клинических ветеринарных пациентов станет регулярным, необходимо провести серьезное исследование с правильным подбором случаев.
Радиочастотная абляция (РЧА/RFA), регионарная химиотерапия, эмболизация и химиоэмболизация являются методами интервенционной онкологии, которые были описаны при лечении легочной неоплазии.
РЧА – метод местного воздействия на опухоль с помощью высокой температуры, создаваемой высокочастотными радиоволнами. В центр опухолевой ткани вводят электрод, через который подают высокочастотный ток, вызывающий усиленные колебательные движения ионов и высвобождение энергии в виде тепла. Высокая температура приводит к коагуляционному некрозу в определенной области37,39,40. Цель метода состоит в том, чтобы создать область некроза непосредственно самого новообразования и дополнительно на 360° вокруг неопластического поражения, включая краевой отступ непораженной ткани, равный 10 мм37,39. Данной процедуре (с чрескожным доступом под контролем КТ) были подвержены 14 пациентов с экспериментально индуцированной трансмиссивной венерической опухолью легкого (всего 14 новообразований)30. Общие и гистопатологические оценки материала, взятого из пораженных долей легкого, продемонстрировали полный термический коагуляционный некроз всех обработанных поражений. Ни у одной собаки не было выявлено жизнеспособной опухоли.
Регионарная химиотерапия была разработана с целью повышения эффективности химиотерапевтических агентов и снижения побочных эффектов31. Регионарная доставка химиопрепаратов позволяет увеличить их концентрацию в новообразовании путем селективной катетеризации и снабжения опухолевой артерии31. Регионарные методы, включающие введение химиопрепаратов в бронхиальные и легочные артерии, были описаны в нескольких исследованиях, проведенных с участием людей31,32,41. Недавнее исследование показало, что значительно более высокие концентрации химиотерапевтических агентов (гемцитабин и карбоплатин) были отмечены в легочной ткани, которая была обработана методом регионарной селективной перфузии легочной артерии, по сравнению с концентрациями после внутривенного введения в экспериментальной модели. Как сообщалось ранее, показания для этого лечения еще предстоит определить в ветеринарии.
Прогноз
Установлено, что у собак с клиническими признаками на момент выявления новообразования легкого временные интервалы между развитием заболевания (DFI - безрецидивный интервал, т.е. промежуток времени между первичным лечением злокачественного новообразования и первым признаком рецидива опухоли) и временем выживания значительно меньше по сравнению с теми животными, у которых это новообразование было обнаружено случайно25. Это, в свою очередь, говорит в пользу разработки ранних гериатрических скринингов, которые могли бы помочь в выявлении бессимптомно протекающих заболеваний.В одном исследовании было установлено, что собаки с хорошо дифференцированными опухолями жили дольше, чем собаки с умеренно или плохо дифференцированными опухолями25. Аналогичным образом гистологическая степень злокачественности является прогностическим показателем результатов выживаемости у кошек. Медиана выживаемости (median survival time; MST) у кошек, перенесших хирургическую резекцию новообразований легких, составляла 2,5 месяца и 23 месяца для гистологически плохо дифференцированных и хорошо дифференцированных опухолей соответственно.
По результатам еще одного исследования, где оценивалось влияние нескольких переменных на ремиссию и выживаемость у собак с первичными опухолями легкого, было выявлено, что животные, у которых удалось успешно удалить все макроскопически различаемые новообразования, жили значительно дольше тех пациентов, у которых развились послеоперационные осложнения, возможно, сыгравшие ведущую роль в малигнизации процесса и ухудшении состояния животных по основному диагнозу33. Факторы, значительно связанные с ремиссией, включали ограниченную степень поражения первичной опухоли, наличие метастазов в регионарных лимфатических узлах и отсутствие метастатической болезни33.
В отдельном исследовании 15 собак были отмечены тенденции увеличения продолжительности жизни у собак с аденокарциномой (по сравнению с плоскоклеточной карциномой), с периферическими поражениями (по сравнению с поражениями, в которые вовлечена целая доля) и с объемом опухоли менее 100 см3 (по сравнению с объемом, превышавшим 100 см3)12. Собаки без клинических признаков на момент постановки диагноза имели среднее время выживания (MST), составлявшее 545 дней, по сравнению с 240 днями у собак с клиническими признаками11.
T-стадирование опухоли также является прогностической для MST. У животных с наличием одиночных (T1), множественных (T2) и инвазивных (T3) опухолей MST составляла 26, 7 и 3 месяца соответственно25. У собак с метастазированием в лимфатические узлы MST составляла 1 месяц по сравнению с собаками без поражения лимфатических узлов (MST составила в среднем 15 месяцев). В другом исследовании было выявлено, что у собак с увеличением лимфатических узлов, диагностированным до операции, медиана выживаемости составляла в среднем 60 дней, тогда как собаки без увеличения лимфатических узлов имели MST - 285 дней33. Аналогичная тенденция была отмечена в более позднем исследовании, в котором у собак с лимфаденопатией MST составляла 126 дней по сравнению с MST, равной 289 дням, у животных без лимфаденопатии14.
У собак, достигших ремиссии за счет полноценной хирургической операции без оставления макроскопически определяемых новообразований, MST составляла 330 дней по сравнению с 28 днями у тех пациентов, у которых по тем или иным причинам не могли быть достигнуты чистые хирургические границы либо полностью удалены все новообразования33.
Первичные опухоли легких редко встречаются у собак, тогда как легочные метастатические новообразования – распространенное явление.
Продолжение в следующем номере
Список литературы:
- Brodey RS, Craig PH. Primary pulmonary neoplasms in the dog: a review of 29 cases, J Am Vet Med Assoc 147:1628–1643, 1965.
- Nielsen SW, Horava A. Primary pulmonary tumors of the dog. A report of sixteen cases, Am J Vet Res 21:813–830, 1960.
- Moulton JE, von Tscharner C, Schneider R. Classification of lung carcinomas in the dog and cat, Vet Pathol 18:513–528, 1981.
- D’Costa S, Yoon B-I, Kim DY, et al. Morphologic and molecular analysis of 39 spontaneous feline pulmonary carcinomas, Vet Pathol, 2011.
- Dorn CR, Taylor DO, Frye FL, et al. Survey of animal neoplasms in Alameda and Contra Costa Counties, California. I. Methodology and description of cases, J Natl Cancer Inst 40:295–305, 1968.
- Dobson JM, Samuel S, Milstein H, et al. Canine neoplasia in the UK: estimates of incidence rates from a population of insured dogs, J Small Anim Pract 43:240–246, 2002.
- Hahn FF, Muggenburg BA, Griffith WC. Primary lung neoplasia in a beagle colony, Vet Pathol 33:633–638, 1996.
- Griffey SM, Kraegel SA, Madewell BR. Rapid detection of K-ras gene mutations in canine lung cancer using single-strand conformational polymorphism analysis, Carcinogenesis 19:959–963, 1998.
- Stunzi H, Head KW, Nielsen SW. Tumours of the lung, Bull World Health Organ 50:9–19, 1974.
- Meuten DJ. Tumors in domestic animals, ed 4, Ames, Iowa, 2002, Iowa State University Press.
- McNiel EA, Ogilvie GK, Powers BE, et al. Evaluation of prognostic factors for dogs with primary lung tumors: 67 cases (1985-1992), J Am Vet Med Assoc 211:1422–1427, 1997.
- Mehlhaff CJ, Leifer CE, Patnaik AK, et al. Surgical treatment of primary pulmonary neoplasia in 15 dogs, J Am Anim Hosp Assoc 20:5, 1984.
- Ogilvie GK, Haschek WM, Withrow SJ, et al. Classification of primary lung tumors in dogs: 210 cases (1975-1985), J Am Vet Med Assoc 195:106–108, 1989.
- Paoloni MC, Adams WM, Dubielzig RR, et al. Comparison of results of computed tomography and radiography with histopathologic findings in tracheobronchial lymph nodes in dogs with primary lung tumors: 14 cases (1999-2002), J Am Vet Med Assoc 228:1718–1722, 2006.
- Brodey RS. Hypertrophic osteoarthropathy in the dog: a clinicopathologic survey of 60 cases, J Am Vet Med Assoc 159:1242– 1256, 1971.
- Halliwell WH, Ackerman N. Botryoid rhabdomyosarcoma of the urinary bladder and hypertrophic osteoarthropathy in a young dog, J Am Vet Med Assoc 165:911–913, 1974.
- Caywood DD, Kramek BA, Feeney DA, et al. Hypertrophic osteopathy associated with a bronchial foreign body and lobar pneumonia in a dog, J Am Vet Med Assoc 186:698–700, 1985.
- Liptak JM, Monnet E, Dernell WS, et al. Pulmonary metastatectomy in the management of four dogs with hypertrophic osteopathy, Vet Comp Oncol 2:1–12, 2004.
- Grillo TP, Brandao CV, Mamprim MJ, et al. Hypertrophic osteopathy associated with renal pelvis transitional cell carcinoma in a dog, Can Vet J 48:745–747, 2007.
- Hawkins EC, DeNicola DB, Plier ML. Cytological analysis of bronchoalveolar lavage fluid in the diagnosis of spontaneous respiratory tract disease in dogs: a retrospective study, J Vet Intern Med 9:386–392, 1995.
- Liptak JM, Monnet E, Dernell WS, et al. Pneumonectomy, four case studies and a comparative review, J Small Anim Prac 45:441–447, 2004.
- DeVita VT, Lawrence TS, Rosenberg SA. DeVita, Hellman, and Rosenberg’s cancer: principles & practice of oncology, ed 8, Philadelphia, 2008, Wolters Kluwer/Lippincott Williams & Wilkins.
- Ogilvie GK, Reynolds HA, Richardson RC, et al. Phase II evaluation of doxorubicin for treatment of various canine neoplasms, J Am Vet Med Assoc 195:1580–1583, 1989.
- Ogilvie GK, Obradovich JE, Elmslie RE, et al. Efficacy of mitoxantrone against various neoplasms in dogs, J Am Vet Med Assoc 198:1618–1621, 1991.
- Poirier VJ, Burgess KE, Adams WM, et al. Toxicity, dosage, and efficacy of vinorelbine (Navelbine) in dogs with spontaneous neoplasia, J Vet Intern Med 18:536–539, 2004.
- Chabner B, Longo DL. Cancer chemotherapy and biotherapy: principles and practice, ed 4, Philadelphia, 2006, Lippincott Williams & Wilkins.
- Hershey AE, Kurzman ID, Forrest LJ, et al. Inhalation chemotherapy for macroscopic primary or metastatic lung tumors: proof of principle using dogs with spontaneously occurring tumors as a model, Clin Cancer Res 5:2653–2659, 1999.
- Khanna C, Vail DM. Targeting the lung: preclinical and comparative evaluation of anticancer aerosols in dogs with naturally occurring cancers, Curr Cancer Drug Targets 3:265–273, 2003.
- London CA, Hannah AL, Zadovoskaya R, et al. Phase I dose- escalating study of SU11654, a small molecule receptor tyrosine kinase inhibitor, in dogs with spontaneous malignancies, Clin Cancer Res 9:2755–2768, 2003.
- Ahrar K, Price RE, Wallace MJ, et al. Percutaneous radiofrequency ablation of lung tumors in a large animal model, J Vasc Interv Radiol 14:1037–1043, 2003.
- Muller H, Guadagni S. Regional chemotherapy for carcinoma of the lung, Surg Oncol Clin N Am 17:895–917, 2008.
- Van Putte BP, Grootenboers M, van Boven WJ, et al. Selective pulmonary artery perfusion for the treatment of primary lung cancer: Improved drug exposure of the lung, Lung Cancer 65:208–213, 2009.
- Ogilvie GK, Weigel RM, Haschek WM, et al. Prognostic factors for tumor remission and survival in dogs after surgery for primary lung tumor: 76 cases (1975-1985), J Am Vet Med Assoc 195:109–112, 1989.
- Polton GA, Brearley MJ, Powell SM, et al. Impact of primary tumour stage on survival in dogs with solitary lung tumours, J Small Anim Pract 49:66–71, 2008.
- Jemal A, Center MM, DeSantis C, et al. Global patterns of cancer incidence and mortality rates and trends, Cancer Epidemiol Biomarkers Prev 19:1893–1907, 2010.
- G. Polton, R. Finotello, S. Sabattini, F. Rossi, P. Laganga, M. E. Vasconi, A. Barbanera, K. Stiborova, C. Rohrer Bley, L. Marconato. Survival analysis of dogs with advanced primary lung carcinoma treated by metronomic cyclophosphamide, piroxicam and thalidomide. Vet Comp Oncol. September 2018;16(3):399-408.
- Rose SC, Thistlethwaite PA, Sewell PE, et al. Lung cancer and radiofrequency ablation, J Vasc Interv Radiol 17:927–951; quiz 951, 2006.
- Okuma T, Matsuoka T, Yamamoto A, et al. Frequency and risk factors of various complications after computed tomography-guided radiofrequency ablation of lung tumors, Cardiovasc Intervent Radiol 31:122–130, 2008.
- Crocetti L, Lencioni R. Radiofrequency ablation of pulmonary tumors, Eur J Radiol 75:23–27, 2010.
- Duncan M, Wijesekera N, Padley S. Interventional radiology of the thorax, Respirology 15:401–412, 2010.
- Grootenboers MJ, Schramel FM, van Boven WJ, et al. Selective pulmonary artery perfusion followed by blood flow occlusion: new challenge for the treatment of pulmonary malignancies, Lung Cancer 63:400–404, 2009.
- Poirier VJ, Burgess KE, Adams WM, et al: Toxicity, dosage, and efficacy of vinorelbine (Navelbine) in dogs with spontaneous neoplasia, J Vet Intern Med 18:536–539, 2004.

 vetpeterburg
vetpeterburg Ветеринарный Петербург
Ветеринарный Петербург